Van der Waalsove sile
From Wikipedia, the free encyclopedia
Remove ads
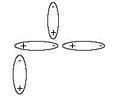
Van der Waalsove sile[1] su relativno slabe sile koje postoje između nepolarnih molekula. Nazivaju se još i Londonove disperzione sile. Disperzione sile između molekula daleko su slabije od kovalentnih veza. Nastaju uslijed kretanja elektrona duž veze, pri čemu će u nekom momentu jedna strana molekule imati veću gustinu elektrona od druge. Na taj način nastaje inducirani dipol.
Remove ads
Primjer
Alkani su nepolarne molekule, zbog male razlike u elektronegativnosti između ugljika i vodonika. Zbog toga molekule alkana nemaju parcijalne naboje na molekulama. Zbog toga, jačina van der Waalsovih sila zavisi od veličine kontaktne površine između molekula. Izobutan (tačka ključanja -10,2 °C) i butan (tačka ključanja -0,6 °C) su očigledni primjeri. Molekula butana ima veću dodirnu površinu od molekule izobutana, pa su van der Waalsove sile jače, što uzrokuje višu tačku ključanja.[2]
Remove ads
Također pogledajte
Reference
Vanjski linkovi
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads