CRISPR
From Wikipedia, the free encyclopedia
Remove ads
CRISPR jsou segmenty nahromaděných pravidelně rozmístěných krátkých palindromických repetic (Clustered Regularly Interspaced Short Palindromic Repeats),[1] jsou to úseky prokaryotické DNA obsahující krátké repetice nukleotidů. Každá z repetic je následována krátkými segmenty tzv. spacer DNA, získanými při předchozích setkáních s příslušnými fágy nebo plazmidy.[2]

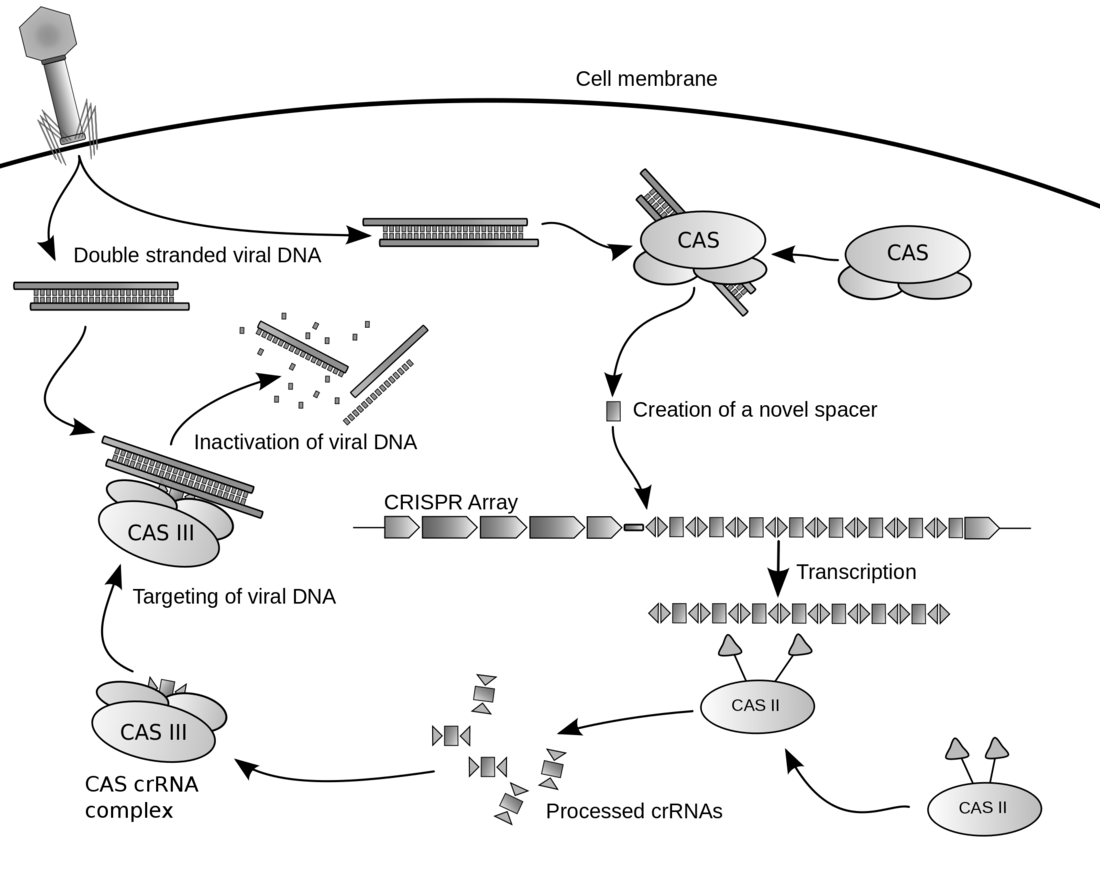
CRISPR / Cas systém je prokaryotický imunitní systém, zajišťující rezistenci vůči cizím genetickým elementům, jako jsou plazmidy nebo fágy,[3][4] a představuje tedy formu získané imunity. Spacerová DNA tyto exogenní genetické elementy rozpozná a deaktivuje způsobem analogickým s mechanismem RNA interference v eukaryotických organismech.[5] CRISPR lokusy již byly objeveny u přibližně 40% osekvenovaných bakterií a u 90% archeí.[6] Technologie CRISPR interference má enormní potenciál k uplatnění, včetně pozměňování lidské zárodečné linie, zvířat (i dalších organismů) nebo modifikace genů potravinářských plodin. Doručením proteinu Cas9 a příslušné naváděcí RNA do buňky lze genom cílového organismu rozstřihnout v jakémkoli požadovaném místě.[7][8][9] CRISPRy ve spojení se specifickými endonukleázami, určenými k editování genomu či cílené regulaci genů, již byly otestovány v rozličných organismech[10]. Z etického hlediska se jeví jako znepokojivá zejména možnost editace lidské zárodečné linie.[11]
Remove ads
Historie
CRISPR je přirozenou součástí bakteriálních procesů. Bakterie mají schopnost začleňovat cizí DNA a dokonce i účelně získávat poškozenou DNA přímo ze svého okolního prostředí.[12] Nahromaděné repetice byly poprvé popsány v roce 1987 u bakterie Escherichia coli na Univerzitě v Osace, vědcem Yoshizumim Ishinou, v té době ovšem jejich funkce nebyla známa.[13] Nezávisle na tom byly tyto repetice pozorovány také španělským badatelem Franciscem Mojicou v roce 1993[14], který je nazval krátkými pravidelně rozmístěnými repeticemi (SRSR).[15] V roce 2000 byly podobné repetice identifikovány u dalších zástupců bakterií a archeí.[15] Na Mojicův návrh byly SRSR roku 2002 přejmenovány na CRISPR.[16][17] Poprvé vyvstalo podezření, že by CRISPR lokusy mohly být zodpovědné za zprostředkování adaptivní imunity u mikrobů.[16][18] Práce zahrhující tyto hypotézy byla prvotně odmítnuta celou řadou vysoce impaktovaných žurnálů.[16][19][20] Byla objevena řada genů, asociovaných s CRISPRovýmy repeticemi, pojmenovaných Cas, neboli CRISPR-associated genes (s CRISPRem-asociované geny). Cas geny kódují nukleázy nebo helikázy, což jsou enzymy, které stříhají (nukleázy) nebo rozvolňují (helikázy) dvoušroubovici DNA[21]. V roce 2005, tři nezávislé výzkumné skupiny prokázaly, že některé DNA spacery z CRISPR lokusu jsou odvozeny z fágové a extrachromozomální DNA, jako jsou plazmidy.[22][23][24] Spacery byly identifikovány jako fragmenty DNA pocházející z virů, které již dříve napadly danou bakteriální buňku. Původ DNA spacerů byl známkou toho, že by CRISPR/Cas systém mohl hrát roli v adaptivní imunitě bakterií.[25][26] Koonin a jeho tým navrhli, že DNA spacery slouží jako templáty pro transkripci RNA molekul analogicky systému zvanému RNA interference uplatňovanému v eukaryotických buňkách[27]. V roce 2007, Barrangou, Horvath (odborníci potravinového průmyslu v Daniscu) a skupina Moineau na Université Laval v Kanadě ukázali, že lze využít spacerovou DNA ke změně rezistence Streptococcus thermophilus vůči útoku fágů.[27] V roce 2012 bylo poprvé ukázáno, že CRISPR může být využit jako nástroj genového inženýrství pro editaci genů v lidské buněčné kultuře.[28][29] Od té doby byl již systém úspěšně vyzkoušen v široké škále organismů od kvasinek (S. cerevisiae),[30] Dania pruhovaného (D. rerio)[31], octomilky (D. melanogaster),[32] Axolotl (A. mexicanum),[33] hlístice (C. elegans),[34] rostlin,[35] myší,[36] opic[37] až po lidská embrya[38]. CRISPR byl modifikován do podoby programovatelných transkripčních faktorů, které vědcům umožňují přesně zacílit a pak aktivovat nebo umlčet specifické geny.[39] Nyní jsou již k dispozici knihovny desítek tisíc ověřených naváděcích RNA.[40] Soudní dvůr Evropské unie však roku 2018 metodu postavil na úroveň GMO.[41]
Remove ads
Cas9
Jennifer Doudna a Emmanuelle Charpentier (nezávisle na sobě) zkoumaly s CRISPRem-asociované proteiny, ve snaze lépe porozumět mechanismu využití DNA spacerů v imunitní obraně bakterií.[42] Obě vědkyně se zaměřily na jednodušší CRISPR systém, který využívá bílkovinu zvanou Cas9. Zjistily, že bakterie reagují na napadení fágem přepisem příslušného DNA spaceru a přilehlých palindromických sekvencí do dlouhé molekuly RNA. Buňka pak použije tracrRNA (trans-activating crRNA) a protein Cas9 k rozstříhání této dlouhé RNA molekuly na kratší kousky zvané crRNA (CRISPR RNA)[40]. Cas9 je nukleáza, enzym, specializovaný pro stříhání DNA. Má dvě aktivní „stříhací“ místa (HNH a RuvC), jeden pro každé vlákno dvoušroubovice DNA. Bylo prokázáno, že lze jedno či obě tato aktivní místa deaktivovat při zachování schopnosti Cas9 vyhledat a navázat cílovou sekvenci v DNA. V roce 2012, Doudna a Charpentier (nyní již ve společné vědecké skupině) zkombinovaly tracrRNA a crRNA do jediné hybridní „guide“ RNA molekuly (gRNA), která je v komplexu s Cas9 schopna přesně zacílit a rozstřihnout libovolnou sekvenci v DNA. Ve své studii navrhly využití takto uměle sestavené naváděcí RNA jako prostředku využitelného k editaci genů.[43]
Remove ads
Předchůdci CRISPR/Cas9 systému
Na přelomu tisíciletí, vědci vyvinuli tzv. Zinc-finger nukleázy (nespecifické nukleázy spojené se zinkovými prsty, syntetickými proteiny, jejichž DNA-vazebné domény umožňují rozeznávat specifické sekvence v DNA) umožňující vytvářet dvojřetězcové zlomy v DNA na předem vybraných místech. V roce 2010, s objevem syntetických nukleáz zvaných TALENy, došlo ke značnému zjednodušení a zpřesnění zacilování na konkrétní místa v sekvenci DNA. Zinc-finger nukleázy i TALENy vyžadují navržení a syntézu proteinů, které dokáží rozeznat cílovou sekvenci na bázi interakce protein-DNA, což je finančně i časově náročnější proces, než je tomu při využití komplementárního párování RNA-DNA. CRISPR vyžaduje pouze tvorbu krátkých sekvencí RNA.[44]
Odkazy
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads