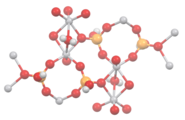
Můstkový ligand
ligand, který propojuje dvě nebo více koordinačních center From Wikipedia, the free encyclopedia
Remove ads
V koordinační chemii se jako můstkový ligand označuje ligand, který je navázán na dva nebo více atomů, často iontů kovů.[1] Tyto ligandy mohou být jednoatomové i víceatomové. Jako můstkové ligandy mohou fungovat mnohé komplexní organické sloučeniny, a tak se takto označují obvykle jen malé ligandy, jako jsou pseudohalogenidy, případně ligandy vytvořené přímo za účelem propojení dvou kovů.

Při pojmenovávání komplexů, ve kterých jeden atom vytváří můstek mezi kovy, se před název ligandu přidává řecké písmeno mí (μ),[2] s číslem v dolním indexu, který označuje počet atomů kovů ligandu. μ2 se obvykle zapisuje jednodušeji jako μ. Při popisu komplexů je třeba nezaměňovat μ za η (éta), jež slouží k označení hapticity. Ligandy nevytvářející můstky se nazývají koncové (terminální) ligandy.
Remove ads
Příklady anorganických můstkových ligandů
Můstek mohou vytvořit téměř všechny ligandy, výjimky představují aminy a amoniak.[3]
K častým anorganickým můstkovým ligandům patří většina běžných aniontů:
Mnoho jednoduchých organických liganů vytváří mezi atomy kovů silné můstky; jako příklady lze uvést organické deriváty výše uvedených ligandů (R = alkyl nebo aryl): OR−, SR−, amido (NR -
2 ), imido (NR2−), fosfido (PR -
2 ) a fosfinidinové ligandy (PR2−).
Remove ads
Sloučeniny
- Sloučeniny obsahující můstkové ligandy
- V tomto komplexu, dimeru (benzen)ruthenium dichloridu, jsou dva chloridové ligandy koncové a dva vytvářejí můstky.
- V komplexu Co3(CO)9(CtBu) vytváří ligand CtBu můstek mezi třemi atomy, i když se tato skutečnost do vzorce obvykle nezapisuje.
- U dodekakarbonylu triželeza vytvářejí dva CO ligandy můstky a zbylých deset jsou koncové ligandy. Koncové a můstkové CO ligandy se rychle vyměňují.
- Dimer chloridu niobičného (NbCl5) obsahuje dva můstkové a osm koncových chloridových ligandů.
- Sloučenina [Au6C(PPh3)6]2+ obsahuje μ6-karbidový ligand,; značka μ se zde většinounepoužívá.
- U oxidu rheniového jsou všechny oxidové ligandy μ2. Tyto oxidové ligandy drží pohromady kovová centra.
- Molekuly chloridu zirkoničitého (ZrCl4) obsahují koncové i dvojnásobně můstkové chloridové ligandy.
- Octan rhodnatý má čtyři octanové skupiny jako můstkové ligands.
- VO(HPO4)*0,5 H2O má dvojici vanadičitých center spojených molekulami vody.[4]
Remove ads
Vazby
U dvojnásobných (μ2-) ligandů se vyskytují čtyřelektronové a dvouelektronové vazebné interakce. Tyto stavy se u prvků vlastní skupiny dají zapsat jako [Me2Al(μ2-Cl)2 a [Me2Al(μ2-Me)2. Tuto analýzu ztěžují možné vazby mezi kovy. Výpočetními studiemi bylo potvrzeno, že u většiny sloučenin s kovy oddělenými můstkovými ligandy vazby kov–kov nejsou přítomny, například nonakarbonyl diželeza, Fe2(CO)9 neobsahuje vazby železo–železo a nachází se v něm tricentrické dvouelektronové vazby mezi třemi můstkovými CO ligandy.[5]

Polyfunkční ligandy
Polyfunkční ligandy se mohou na kovy navázat různými způsoby a mohou tak i různě vytvářet můstky mezi nimi, například sdílením jednoho nebo i více atomů. Příklady takových ligandů jsou oxoanionty CO 2−
3 a podobné karboxyláty, dále PO 3−
4 a polyoxometaláty. Tyto můstkové dvojice kovů jsou obsaženy například v některých organofosforečných sloučeninách, jako je bis(difenylfosfino)methan (dppm). Ph2PCH2PPh2.
Remove ads
Odkazy
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads