Metalace
chemické reakce, při kterých se navazují atomy kovu na organické sloučeniny From Wikipedia, the free encyclopedia
Remove ads
Metalace jsou chemické reakce, při kterých se navazují atomy kovu na organické sloučeniny, obvykle přitom nahrazují atomy halogenů. V laboratořích se obvykle používají k aktivaci organických molekul v průběhu vytváření vazeb C—X (kde X je většinou uhlík, kyslík nebo dusík), jež jsou potřebné k tvorbě dalších organických sloučenin.
Metalovaná činidla mívají nejčastěji využití při nukleofilních substitucích, reakcích s přenosem jednoho elektronu a redoxních reakcích funkčních skupin na jiných molekulách (jako jsou ketony, aldehydy a halogenalkany). Metalované molekuly se také účastní acidobazických reakcí, kde organokovové činidlo deprotonuje organickou molekulu za vzniku nového organokovového činidla.
Nejrozšířenější skupinou metalovaných sloučenin jsou organolithné sloučeniny a Grignardova činidla; v laboratořích i průmyslu se však používají i jiné organokovové sloučeniny, například organozinečnaté sloučeniny.
Remove ads
Historie
Metalaci v laboratoři poprvé pozoroval Edward Frankland při syntéze diethylzinku v roce 1849.[1]
Tento objev vedl k vývoji organokovových sloučenin odvozených od jiných kovů,[2] které ovšem měly jen omezené využití v laboratořích, protože byly drahé a značně pyroforické. Rozvoj metalací (převážně transmetalací) nastal až po Grignardovu objevu přípravy organohořečnatých halogenidů přímo z kovového hořčíku a organohalogenidů.[3]
Tato organohořečnatá činidla našla díky možnosti provádět metalace mnoha různých substrátů široké využití v laboratořích.[4]
Organolithné sloučeniny byly poprvé připraveny roku 1917,[5] ovšem jejich využívání se rozšířilo až poté, kdy Karl Ziegler, Henry Gilman a Georg Wittig vyvinuly jednodušší metody jejich přípravy.[6]
Po objevu těchto vylepšení došlo k výraznému nárůstu zájmu o tyto sloučeniny, protože jsou většinou reaktivnější než organohořečnatá činidla. První použití organolithného činidla k metalaci bylo popsáno v roce 1928, šlo o reakci fluorenu s ethyllithiem.[7]
Remove ads
Reaktivita a použití
Mnoho jednou metalovaných sloučenin lze zakoupit v pevném skupenství i jako roztoky, přičemž roztoky jsou dostupné v řadě různých rozpouštědel i koncentrací. Také je lze připravit v laboratoři jako in situ meziprodukty nebo jako roztoky.
Reaktivita metalovaných sloučenin
Velký rozdíl v elektronegativitě atomů uhlíku a kovu u většiny metalovaných sloučenin způsobuje značnou polaritu vazby uhlík-kov. Vysoká polarita vazby a z toho vyplývající vysoká elektronová hustota okolo metalovaného uhlíkového atomu způsobuje, že se povaha vazby blíží vazbě iontové. Metalované sloučeniny tak bývají dobrými nukleofily a silnými zásadami.
Metalované sloučeniny mají největší využití v organické syntéze, kde slouží jako nukleofily při nukleofilních substitucích, jako silné zásady při deprotonacích, iniciátory polymerizací a jako výchozí materiály pro přípravu dalších organokovových sloučenin transmetalačními reakcemi.
Stericky narušované metalované sloučeniny, například komplexy n-butyllithia se často používají jako superzásady či iniciátory polymerizací, protože jimi vyvolávané sterické efekty narušují možnosti sloučenin přiblížit se k nukleofilům dostatečně blízko na provedení nukleofilního ataku. Sloučeniny bez těchto vlastností, například methyllithium a alkylhořečnaté halogenidy, se většinou používají jako nukleofily nebo transmetalační činidla, i když jejich silně zásaditá povaha často vyžaduje ochranu zásaditých funkčních skupin nacházejících se v organických molekulách.
Remove ads
Mechanismus
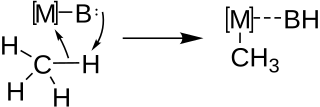
Metalace se obvykle využívá k syntéze složitějších organokovových sloučenin, jako jsou alkynyllithná činidla, z uhlovodíků obsahujících kyselé vodíky. Při mezimolekulárních i vnitromolekulárních metalacích reakce probíhá přes acidobazickou funkcionalizaci vazby C-H párováním kovu (M) se zásadou (B) podle následujícího schématu:
Relativní stabilita konečných produktů závisí na tom, zda je reakce vratná či nevratná a relativní kyselost vazeb C-H v metalovaných molekulách určuje, kam v molekule reaktantu se kov naváže.
První mechanismus metalace, založený na soustředěné metalaci-deprotonaci (CMD), navrhli v roce 1955 S. Winstein a T. G. Traylor na základě elektrofility rtuti při acetolýze difenylrtuti v kyselině octové.[8]
Pozdější mechanistické studie podpořily tento mechanismus u mezimolekulárních i vnitromolekulárních metalací. Všeobecně přijímaný mechanismus je znázorněn níže, jako příklad je zde použita metalace primárního vodíku.[9]
Transmetalace
Podrobnější informace naleznete v článku Transmetalace.
Transmetalace je výměna dvou kovů mezi organickými molekulami prostřednictvím redoxní záměny. Často jde o reakci organolithného činidla se solí kovu.
Organolithné sloučeniny
Podrobnější informace naleznete v článku Organolithné sloučeniny.
Při přípravě jednoduchých organolithných činidel redukcí jednoho ekvivalentu alkyl- nebo arylhalogenidu dvěma ekvivalenty lithia vzniká jeden ekvivalent alkyl- nebo aryllithné sloučeniny a jeden ekvivalent lithného halogenidu.[10]
Reakce probíhá radikálovým mechanismem a pravděpodobně je iniciována jednoelektronovým mechanismem (znázorněným níže).[11]
Podobně může hořčík metalovat organohalogenidy za vzniku Grignardových činidel
Remove ads
Reference
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads