Oxid sodný
chemická sloučenina From Wikipedia, the free encyclopedia
Remove ads
Oxid sodný (Na2O) je jediný oxid sodíku.
Remove ads
Vlastnosti
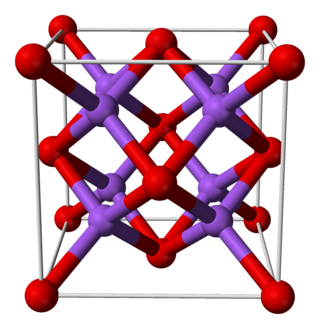
Je to za normálních podmínek bílá krystalická látka.[2] Její krystaly, podobně jako krystaly všech oxidů alkalických kovů, mají tzv. antifluoritovou strukturu, což znamená, že pozice aniontů a kationtů v krystalové mřížce jsou zcela obrácené, než je tomu u fluoridu vápenatého (CaF2). Sodíkové kationty tvoří středy tetraedrů, neboť jsou připojeny na 4 atomy kyslíku, zatímco kyslíkové atomy tvoří středy krychle, neboť jsou navázány na 8 sodíkových iontů.[3][4] Za vysokých teplot se rozkládá na peroxid sodný a sodík.[5]
S vodou bouřlivě reaguje za vzniku hydroxidu sodného[5] (je to vlastně jeho anhydrid):
Na2O + H2O → 2 NaOH |
|
Při kontaktu s očima, pokožkou a sliznicí dýchací soustavy je silně dráždivý a zejména prášková forma může snadno způsobit zdravotní potíže. Vdechnutí většího množství dokonce může vyvolat plicní edém.[5]
Remove ads
Příprava
Tento oxid je možné připravit např. reakcí oxidu dusného se sodíkem:[6]
N2O + 2Na → Na2O + N2 |
|
Taktéž je možné jej připravit tepelným rozkladem uhličitanu sodného:
Na2CO3 → Na2O + CO2 |
|
Použití
Oxid sodný se používá jako přísada při výrobě skla pro snížení teploty tavení oxidu křemičitého, který je hlavní složkou skla.
Reference
Literatura
Externí odkazy
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads