Oxid uhelnatý
jedovatá chemická sloučenina From Wikipedia, the free encyclopedia
Remove ads
Oxid uhelnatý (starší terminologií kysličník uhelnatý) je bezbarvý jedovatý plyn bez chuti a zápachu, nedráždivý. Ve vodě je málo rozpustný. Je obsažen ve svítiplynu, v generátorovém a ve vodním plynu; má silně redukční vlastnosti. V přírodě je přítomen v nepatrném množství v atmosféře, kde vzniká především fotolýzou oxidu uhličitého působením ultrafialového záření, jako produkt nedokonalého spalování fosilních paliv i biomasy. Je také obsažen v sopečných plynech. V mezihvězdném prostoru se vyskytuje ve značném množství. Byl nalezen i v atmosféře Marsu (0,08 %) a spektroskopicky prokázán v komě komet.
Remove ads
Vznik
Vzniká z kyslíkatých organických látek rozkladem při vysokých teplotách. Např. při koksování uhlí. Nad 600 °C vzniká i při spalování ochotněji než oxid uhličitý.
Ve vysoké peci se získává vysokoteplotním spalováním koksu:
- 2 C + O2 → 2 CO
Endotermní reakcí vodní páry s koksem za vysokých teplot se vyráběl vodní plyn jako ušlechtilé palivo nebo zdroj vodíku:
- C + H2O → CO + H2
Vzniká také při výrobě vodíku parním reformováním methanu endotermní reakcí okolo 1000 °C:
- CH4 + H2O → 3 H2 + CO
Následně se ale spotřebovává konverzí pod 600 °C, kdy redukuje vodní páru:
- CO + H2O → H2 + CO2
V nepatrném množství vzniká i metabolickými procesy v živých organismech a proto je obsažen ve stopových množstvích ve vydechovaném vzduchu z plic.
Remove ads
Vlastnosti
S kyslíkem hoří namodralým plamenem na oxid uhličitý:
- 2 CO + O2 → 2 CO2
za uvolnění značného množství tepla. Ve směsi, obsahující od 12,5 do 74,2 % [2] oxidu uhelnatého ve vzduchu, reakce probíhá jako výbuch. I při nižší koncentraci tato reakce probíhá dobře na katalyzátoru výfukových plynů.
CO má podobnou hustotu jako vzduch, nepatrně nižší (97 %).
Využití
Oxid uhelnatý se dříve používal jako plynné palivo (například součást svítiplynu). Jeho směs s vodíkem (vodní plyn) byl jedním z meziproduktů používaných v těžkém chemickém a potravinářském[3] průmyslu. Při výrobě železa vzniká oxid uhelnatý z uhlíku v koksu a spolu s ním funguje jako redukční činidlo.
Zdroje oxidu uhelnatého a jeho výskyt v ovzduší
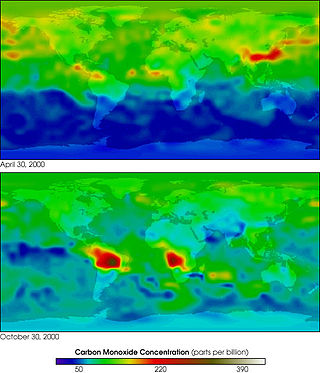
Vzhledem k jedovatosti je jednou z významných znečišťujících látek. Vzniká při vysokoteplotním spalování uhlíku a organických látek. Je emitován např. automobily, lokálními topeništi, energetickým a metalurgickým průmyslem.
CO vzniká zejména pokud:
- je teplota spalování příliš nízká, než aby mohlo dojít k úplné oxidaci pohonných látek na oxid uhličitý,
- čas hoření ve spalovací komoře je příliš krátký,
- není k dispozici dostatek kyslíku.
Díky povinnému zavedení řízených katalyzátorů u vozidel s benzínovými motory se emise oxidu uhelnatého v poslední době snižují.
V roce 2005 v České republice nepřekračovaly pozaďové koncentrace 300 µg/m3. V Praze činily roční aritmetické průměry v oblastech zatížených dopravou přibližně 1.000 µg/m3.[4]
Při používání zemního plynu k vaření v domácnostech je koncentrace CO v domácím ovzduší průměrně cca 2.900 µg/m3 [5].
Kouření
Významným zdrojem oxidu uhelnatého je kouření. Lidé kouřící cca 20 cigaret denně mají asi 4 až 7 % krevního hemoglobinu zablokováno působením CO.[4] Při pasivním kouření je člověk vystaven koncentracím okolo 1.700 µg/m3 [5].
Remove ads
Účinky na živé organismy
Toxicita
Oxid uhelnatý je značně jedovatý; jeho jedovatost je způsobena silnou afinitou k hemoglobinu (krevnímu barvivu), s nímž vytváří karboxyhemoglobin (COHb), čímž znemožňuje přenos kyslíku v podobě oxyhemoglobinu z plic do tkání. Vazba oxidu uhelnatého na hemoglobin je přibližně dvousetkrát silnější než kyslíku, a proto jeho odstranění z krve trvá mnoho hodin až dní. Příznaky otravy se objevují již při přeměně 10 % hemoglobinu na karboxyhemoglobin.
Otrava oxidem uhelnatým
Podrobnější informace naleznete v článku Otrava oxidem uhelnatým.
Oxid uhelnatý blokuje přenášení kyslíku krví, neboť jeho vazba s hemoglobinem je 200× až 300× pevnější než vazba kyslíku a z hemoglobinu se stává karboxyhemoglobin. Otrava CO se vyskytuje např. v uzavřených prostorech, kde běží spalovací motory nebo při špatném odvětrání plynových spotřebičů. První pomoc spočívá v přerušení kontaktu (vyvětrat, vynést z prostoru), dále podání kyslíku a pokud došlo k zástavě oběhu, je třeba resuscitovat.
Oxidem uhelnatým (ve svítiplynu) se otrávil například skladatel a zpěvák Jiří Šlitr.[6]
Signalizační molekula
Oxid uhelnatý patří spolu s oxidem dusnatým a sulfanem ke gasotransmiterům; působí (podobně jako oxid dusnatý) jako relaxant na hladkosvalové buňky ve stěnách cév (vasodilatační účinek). Oxid uhelnatý vzniká endogenně degradací hemu hemoxygenázou (HMOX), což vede k fyziologickým koncentracím v krvi ve vysokém mikromolárním rozmezí ve formě vázané na hemoglobin známé jako karbonylhemoglobin (COHb).
Remove ads
Odkazy
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads






