Kompressibilitet  er et mål for den relative volumenændring, når trykket
er et mål for den relative volumenændring, når trykket  på et materiale ændres. For et volumen
på et materiale ændres. For et volumen  er kompressibiliteteten givet ved:
er kompressibiliteteten givet ved:

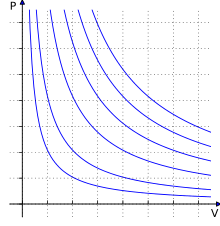
Et pV-diagram med isotermer for en idealgas. Når trykket stiger, falder volumenet, og den isoterme kompressibilitet er derfor positiv.Der kan her skelnes mellem en isoterm kompressibilitet, hvor temperaturen  holdes konstant
holdes konstant

og en adiabatisk kompressibilitet, hvor entropien er konstant:

Hvis volumenet bliver mindre, når trykket øges, er kompressibiliteten altså positiv.[1]
For fx en idealgas, hvor volumenet i følge idealgasligningen er givet ved[2]

er den isoterme kompressiblitet:

Ved høje tryk er det altså sværere at presse gassen sammen.
En anden interessant relation er, at lydens fart er relateret til den adiabatiske kompressibilitet ved:

hvor  er materialets massedensitet.
er materialets massedensitet.