
Όξινο ανθρακικό ιόν
ανιόν / From Wikipedia, the free encyclopedia
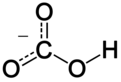
Στην ανόργανη χημεία, διττανθρακικό (IUPAC-συνιστώμενη ονοματολογία: υδρογονανθρακικό (hydrogencarbonate)[2]) είναι μια ενδιάμεση μορφή στην αποπρωτονίωση του ανθρακικού οξέος. Είναι ένα πολυατομικό ανιόν με χημικό τύπο HCO−
3.
Τα διττανθρακικά διαδραματίζουν κρίσιμο βιοχημικό ρόλο στο φυσιολογικό pH ρυθμιστικού συστήματος.[3]
Ο όρος "διττανθρακικό" επινοήθηκε το 1814 από τον Άγγλο χημικό William Hyde Wollaston.[4][5] Το όνομα παραμένει ως εμπειρικό όνομα.
Γρήγορες Πληροφορίες Ονόματα, Αναγνωριστικά ...
 | |
 | |
| Ονόματα | |
|---|---|
| ΟνοματολογίαIUPAC
Υδρογονανθρακικό (Hydrogencarbonate) | |
| ΣυστηματικήΟνοματολογίαIUPAC
Hydroxidodioxidocarbonate(1−)[1] | |
ΆλλαΟνόματα
| |
| Αναγνωριστικά | |
| 71-52-3 | |
| 3DMet | B00080 |
| 3903504 | |
| ChEBI | CHEBI:17544 |
| ChEMBL | ChEMBL363707 |
| ChemSpider | 749 |
| 49249 | |
InChI=1S/CH2O3/c2-1(3)4/h(H2,2,3,4)/p-1 Key: BVKZGUZCCUSVTD-UHFFFAOYSA-M | |
| Jmol 3Δ Πρότυπο | Image |
| KEGG | C00288 |
| PubChem | 769 |
OC([O-])=O | |
| UNII | HN1ZRA3Q20 |
CompTox Dashboard (EPA) |
|
| Ιδιότητες | |
| HCO− 3 | |
| Μοριακή μάζα | 61,0168 g mol−1 |
| log P | −0,82 |
| Οξύτητα (pKa) | 10,3 |
| Βασικότητα (pKb) | 7,7 |
| ΣυζυγέςΟξύ | Ανθρακικό οξύ |
| ΣυζυγήςΒάση | Ανθρακικό ιόν |
Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες (25°C, 100 kPa). | |
| Infobox references | |
Κλείσιμο