παρεντερικό αντιπηκτικό φάρμακο με ταχεία δράση From Wikipedia, the free encyclopedia
Η ηπαρίνη είναι οργανική χημική ένωση (μία γλυκοζαμινογλυκάνη) που αποτελεί φυσικό αντιθρομβωτικό φάρμακο.[1] Χρησιμοποιείται σε ενέσιμη μορφή για την πρόληψη και θεραπεία φλεβικών θρομβώσεων και της πνευμονικής εμβολής.[1] Χορηγείται επίσης ως μέρος της αγωγής για το έμφραγμα του μυοκαρδίου και της ασταθούς στηθάγχης.[1]

Συχνές παρενέργειες της χορηγήσεως ηπαρίνης είναι οι αιμορραγίες και η ηπαρινοεπαγόμενη θρομβοκυτταροπενία.[1] Μεγαλύτερη προσοχή χρειάζεται σε ανθρώπους με νεφρική ανεπάρκεια.[1] Από την άλλη, η ηπαρίνη φαίνεται να είναι ασφαλής για χορήγηση σε εγκύους και θηλάζουσες γυναίκες.[2]
Η φυσική δράση της ηπαρίνης στον υγιή οργανισμό δεν έχει ακόμα αποσαφηνισθεί. Η ουσία αποθηκεύεται συνήθως μέσα στα εκκριτικά κοκκία των μαστοκυττάρων του αίματος και απελευθερώνεται στο αίμα μόνο σε σημεία τραυματισμού των ιστών. Για τον λόγο αυτό έχει υποστηριχθεί ότι ο κύριος ρόλος της ηπαρίνης δεν είναι αντιθρομβωτικός, αλλά η άμυνα σε τέτοιες περιοχές εναντίον των εισβαλλόντων βακτηρίων και άλλων ξένων προς το σώμα παραγόντων.[3] Εκτός από τον ανθρώπινο οργανισμό, η ηπαρίνη ανιχνεύεται σε αρκετά διαφορετικά ζωικά είδη, ακόμα και σε κάποια ασπόνδυλα που δεν διαθέτουν παρόμοιο σύστημα για τη θρόμβωση του αίματος.
Από χημική άποψη, η ηπαρίνη έχει την υψηλότερη πυκνότητα ηλεκτρικού φορτίου από οποιοδήποτε άλλο βιομόριο.[4] Στη φύση η ηπαρίνη είναι πολυμερισμένη με διάφορα μήκη μοριακής αλυσίδας. Η «ηπαρίνη χαμηλού μοριακού βάρους» (Low-Molecular-Weight Heparin, LMWH) έχει υποστεί τεμαχισμό των μακρών αλυσίδων με σκοπό η φαρμακοδυναμική της να γίνει περισσότερο προβλέψιμη.
Η ηπαρίνη περιέχεται στον Κατάλογο Βασικών Φαρμάκων του Παγκόσμιου Οργανισμού Υγείας, ο οποίος περιέχει τις σημαντικότερες φαρμακευτικές ουσίες που χρειάζονται σε ένα βασικό σύστημα υγείας.[5]

Η ηπαρίνη είναι φάρμακο που παράγεται με φυσικό τρόπο στον ανθρώπινο οργανισμό από τα βασεόφιλα κοκκιοκύτταρα και τα μαστοκύτταρα του αίματος.[6] Σε θεραπευτικές δόσεις δρα ως αντιθρομβωτικό, αποτρέποντας τον σχηματισμό θρόμβων και την επέκταση των ήδη υπαρχόντων θρόμβων στο αίμα. Μολονότι η ηπαρίνη δεν διασπά θρόμβους που έχουν ήδη σχηματισθεί (αντίθετα με την πρωτεΐνη PLAT), επιτρέπει στους φυσικούς θρομβολυτικούς μηχανισμούς του σώματος να εργασθούν για τη διάσπαση των θρόμβων αυτών. Γενικά η ηπαρίνη χρησιμοποιείται ως αντιθρομβωτικό στις παρακάτω περιπτώσεις:
Η ηπαρίνη και τα μικρού μοριακού βάρους παράγωγά της (όπως η ενοξαπαρίνη, η δαλτεπαρίνη και η τινζαπαρίνη) προλαμβάνουν τις θρομβώσεις των βαθέων φλεβών και τις πνευμονικές εμβολές σε ανθρώπους που κινδυνεύουν από αυτές[10][11]
Μια σοβαρή παρενέργεια της ηπαρίνης είναι η ηπαρινοεπαγόμενη θρομβοκυτταροπενία (HIT), προκαλούμενη από μία ανοσολογική αντίδραση που καθιστά τα θρομβοκύτταρα στόχο του ανοσοποιητικού συστήματος, με αποτέλεσμα τη μείωσή τους. Αυτή η κατάσταση συνήθως παύει με τη διακοπή της χορηγήσεως ηπαρίνης και γενικώς μπορεί να αποφευχθεί με τη χρήση συνθετικών ηπαρινών. Μια ελαφρά μορφή θρομβοκυτταροπενίας συνδέεται με την έναρξη της χορηγήσεως ηπαρίνης και ανατάσσεται χωρίς να χρειασθεί η διακοπή της ηπαρίνης.
Δύο μη αιμορραγικές παρενέργειες της ηπαρίνης είναι γνωστές. Η πρώτη είναι η άνοδος των επιπέδων της τρανσαμινάσης του ορρού, που έχει αναφερθεί στο 80% των ασθενών που λαμβάνουν ηπαρίνη. Αυτό το φαινόμενο δεν συνδέεται με δυσλειτουργία του ήπατος και εξαφανίζεται μετά τη διακοπή της χορηγήσεως του φαρμάκου. Η άλλη παρενέργεια είναι η υπερκαλιαιμία, που εκδηλώνεται μόλις στο 5 ως 10% των ληπτών ηπαρίνης και οφείλεται στη μείωση της αλδοστερόνης που προκαλεί η ηπαρίνη. Η υπερκαλιαιμία μπορεί να παρουσιαστεί λίγες ημέρες μετά την έναρξη θεραπείας με ηπαρίνη. Σπανιότερα, σε περιπτώσεις χρόνιας χρήσεως ηπαρίνης, μπορεί να εμφανισθούν αλωπεκία ή/και οστεοπόρωση.
Βεβαίως, όπως συμβαίνει με πολλά φάρμακα, υπερβολικές δόσεις ηπαρίνης μπορεί να αποβούν ακόμα και θανατηφόρες. Τον Σεπτέμβριο του 2006 η ηπαρίνη απέκτησε κακή δημοσιότητα όταν τρία πρόωρα βρέφη πέθαναν αφού τους χορηγήθηκαν κατά λάθος υπερβολικές δόσεις ηπαρίνης σε νοσοκομείο της Ινδιανάπολης.[12]
Η ηπαρίνη αντενδείκνυται σε ανθρώπους που κινδυνεύουν από αιμορραγίες (ιδιαίτερα όταν η πίεση του αίματος αυξομειώνεται ανεξέλεγκτα), καθώς και σε περιπτώσεις ασθενειών του ήπατος, εγκεφαλικών επεισοδίων, και βαριάς υπέρτασης.
Η θειική πρωταμίνη (1 mg ανά 100 μονάδες ηπαρίνης που έχει ληφθεί το πολύ 4 ώρες νωρίτερα) έχει χορηγηθεί για την εξουδετέρωση της ηπαρίνης (το μόριό της προσδένεται στο μόριο της ηπαρίνης).[13]
Η ηπαρίνη προσδένεται στον ενζυμικό αναστολέα αντιθρομβίνη III, προκαλώντας του μια μεταβολή που έχει ως αποτέλεσμα την ενεργοποίησή του εξαιτίας αυξήσεως στην ευελιξία του βρόχου τής δραστικής περιοχής του μορίου της.[14] Με τη σειρά της, η ενεργοποιημένη αντιθρομβίνη αδρανοποιεί τη θρομβίνη, τον παράγοντα Xa και άλλες πρωτεάσες. Ο ρυθμός αδρανοποιήσεως αυτών των ενζύμων από την αντιθρομβίνη μπορεί να αυξηθεί μέχρι και στο χιλιαπλάσιο εξαιτίας της ηπαρίνης.[15] Το μόριο της ηπαρίνης προσδένεται στο μόριο της αντιθρομβίνη με μία ειδική ακολουθία θειώσεως πεντασακχαριδίων του μορίου της ηπαρίνης:
GlcNAc/NS(6S)-GlcA-GlcNS(3S,6S)-IdoA(2S)-GlcNS(6S)
Για την αδρανοποίηση της θρομβίνης, το μόριο της θρομβίνης προσδένεται στο πολυμερές της ηπαρίνης σε μία θέση κοντά στο πεντασακχαρίδιο. Η πολύ ηλεκτραρνητική πυκνότητα φορτίου της ηπαρίνης συντελεί στην πολύ ισχυρή ηλεκτροστατική της αλληλεπίδραση με τη θρομβίνη.[4] Ο σχηματισμός τριαδικού συμπλέγματος αντιθρομβίνης, θρομβίνης και ηπαρίνης προκαλεί την αδρανοποίηση της θρομβίνης. Για τον λόγο αυτό, η ηπαρινική δράση κατά της θρομβίνης εξαρτάται από τον πολυμερισμό της ηπαρίνης, καθώς το τριαδικό σύμπλεγμα απαιτεί τουλάχιστον 18 μονάδες σακχαριδίου για τον αποτελεσματικό σχηματισμό του.[16] Αντιθέτως, η δράση της κατά του παράγοντα Xa απαιτεί μόνο τη θέση ενός πεντασακχαριδίου.

Αυτή η διαφορά στο μέγεθος έχει οδηγήσει τις φαρμακοβιομηχανίες στην ανάπτυξη ηπαρινών μικρού μοριακού βάρους (Low-Molecular-Weight Heparin, LMWH) και, πιο πρόσφατα, του fondaparinux ως αντιθρομβωτικών φαρμάκων. Οι LMWH και το fondaparinux στοχεύουν τη δράση του παράγοντα Xa αντί της θρομβίνης. Το fondaparinux είναι συνθετικός πεντασακχαρίτης, του οποίου η μοριακή δομή είναι σχεδόν ταυτόσημη με αυτή της πεντασακχαριδιακής ακολουθίας προσδέσεως της αντιθρομβίνης που βρίσκεται στην πολυμερισμένη ηπαρίνη. Τόσο οι LMWH, όσο και το fondaparinux στοχεύουν στη μείωση των κινδύνων οστεοπορώσεως και ηπαρινοεπαγόμενης θρομβοκυτταροπενίας.
Το «Danaparoid», ένα μίγμα θειικής ηπαρίνης, δερματάνης και χονδροϊτίνης, μπορεί να χρησιμοποιηθεί ως αντιθρομβωτικό σε ασθενείς που έχουν αναπτύξει ηπαρινοεπαγόμενη θρομβοκυτταροπενία. Επειδή το Danaparoid δεν περιέχει ηπαρίνη, ούτε θραύσματα ηπαρίνης, η κοινή αντιδραστικότητά του με τα επαγόμενα από την ηπαρίνη αντισώματα αναφέρεται ως λιγότερο από 10%.[17]
Η δράση της ηπαρίνης μετράται στο εργαστήριο ως «μερικός χρόνος θρομβοπλαστίνης» (aPTT), δηλαδή ένα μέτρο του χρόνου που χρειάζεται το πλάσμα του αίματος για να πήξει.
Η ηπαρίνη χορηγείται παρεντερικά επειδή δεν απορροφάται από τα έντερα εξαιτίας της υψηλής ηλεκτραρνητικότητας και του μεγάλου μεγέθους του μορίου της. Μπορεί να χορηγηθεί με ενδοφλέβια ή υποδόρια ένεση, ενώ οι ενδομυικές ενέσεις αποφεύγονται για να μη δημιουργούνται αιματώματα. Εξαιτίας της βραχείας βιολογικής ημιζωής της, περίπου 1 ώρα, η ηπαρίνη πρέπει να χορηγείται τακτικά ή με συνεχή τρόπο. Το πολυμερές της ηπαρίνης έχει ημιζωή 1 ως 2 ώρες[18], ενώ η LMWH έχει ημιζωή 4 ως 5 ώρες.[19] Η χρήση LMWH επέτρεψε έτσι τη χορήγηση μια φορά την ημέρα. Αν απαιτείται μακροπρόθεσμη αντιθρομβωτική αγωγή, η ηπαρίνη χρησιμοποιείται συχνά μόνο για την έναρξή της, μέχρι που να δράσει κάποιο αντιθρομβωτικό σε χάπι, όπως π.χ. η βαρφαρίνη.
Μικρότερες δόσεις ηπαρίνης έχουν πολύ βραχύτερη ημιζωή από ό,τι μεγαλύτερες δόσεις. Η ηπαρίνη που προσδένεται σε μακροφάγα κύτταρα απορροφάται στο εσωτερικό τους, όπου αποπολυμερίζεται. Επίσης, η ηπαρίνη προσδένεται γρήγορα στα κύτταρα του ενδοθηλίου, κάτι το οποίο αποτρέπει την πρόσδεση στην αντιθρομβίνη, που δίνει την αντιθρομβωτική δράση. Για υψηλότερες δόσεις ηπαρίνης ωστόσο, τα κύτταρα του ενδοθηλίου θα κορεσθούν, οπότε μένει η εκκαθάριση της ουσίας από τα νεφρά, μια πολύ βραδύτερη διαδικασία.[20]

Η φυσική ηπαρίνη είναι ένα πολυμερές, με μοριακό βάρος που κυμαίνεται από 3.000 μέχρι 30.000, με το μέσο μοριακό βάρος των περισσότερων εμπορικών σκευασμάτων ηπαρίνης να κυμαίνεται από 12.000 μέχρι 15.000.[21] Η ηπαρίνη ανήκει στην οικογένεια υδατανθράκων που ονομάζονται γλυκοζαμινογλυκάνες, και αποτελείται από θειωμένη επαναλαμβανόμενη μονάδα (μονομερές) δισακχαριδίου.[22] Οι συνηθέστερες μονάδες δισακχαριδίων φαίνονται στα παρακάτω σχήματα. Το πλέον σύνηθες δισακχαρίδιο αποτελείται από 2-O-θειωμένο ιδουρονικό οξύ και 6-O-θειωμένη, N-θειωμένη γλυκοζαμίνη, την IdoA(2S)-GlcNS(6S). Αυτός ο συνδυασμός αποτελεί το 85% των ηπαρινών που λαμβάνουμε από μοσχαρίσιο πνεύμονα και περί το 75% των ηπαρινών από το χοιρινό έντερο.[23]
Υπό φυσιολογικές συνθήκες οι εστερικές και αμιδικές θειικές ομάδες της ηπαρίνης είναι αποπρωτονιωμένες και έλκουν θετικά φορτισμένα ιόντα, σχηματίζοντας άλατα της ηπαρίνης. Η ηπαρίνη χορηγείται συνήθως με τη μορφή τέτοιων αλάτων.
Μία «θεραπευτική μονάδα» ηπαρίνης (Howell unit) είναι ποσότητα ισοδύναμη με περίπου 0,002 mg καθαρής ηπαρίνης και ορίζεται ως η ποσότητα που κρατά 1 χιλιοστόλιτρο αίματος γάτας ρευστό επί 24 ώρες στους 0 °C.[24]
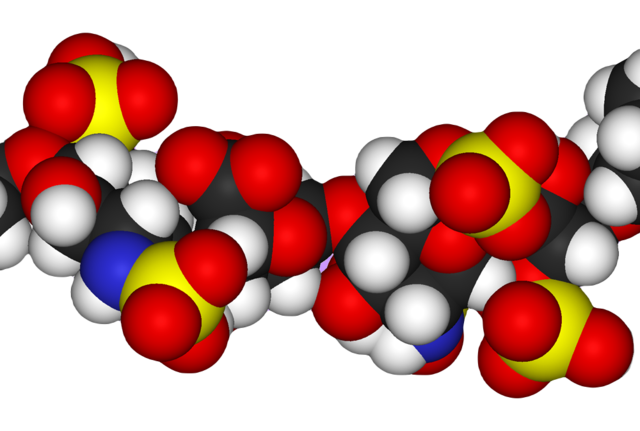
Η τριδιάστατη δομή της ηπαρίνης είναι περίπλοκη, επειδή το ιδουρονικό οξύ μπορεί να εμφανίζεται με τη μία ή την άλλη από δύο διαφορετικές καταστάσεις χαμηλής ενέργειας όταν βρίσκεται στο εσωτερικό ενός ολιγοσακχαριδίου. Η μεταξύ τους ισορροπία επηρεάζεται από την κατάσταση θειώσεως της γειτονικής γλυκοζαμίνης.[25] Παρ' όλα αυτά, η δομή σε διάλυμα ενός δωδεκασακχαριδίου ηπαρίνης που αποτελείται από 6 επαναλαμβανόμενα μονομερή GlcNS(6S)-IdoA(2S) έχει προσδιορισθεί με χρήση συνδυασμού φασματοσκοπίας NMR και τεχνικών μοριακής προτυποποιήσεως.[26].

Στην παραπάνω εικόνα:
Στα μοντέλα αυτά η ηπαρίνη υιοθετεί μια ελικοειδή μορφή, η περιστροφή της οποίας δείχνει τις θειικές ομάδες σε τακτικά διαστήματα περίπου 17 Ώνγκστρεμ (1,7 nm) στην κάθε πλευρά.
Ενζυματικές ή ανόργανες τεχνικές αποπολυμερισμού, ή και συνδυασμός τους, βρίσκονται πίσω από τη μεγάλη πλειονότητα των ανυλύσεων για τη δομή και τη δράση της ηπαρίνης και της θειικής ηπαράνης.
Τα ένζυμα που χρησιμοποιούνται παραδοσιακά για τη διάσπαση της ηπαρίνης παράγονται στη φύση από το βακτηρίδιο του εδάφους Pedobacter heparinus (παλαιότερη ονομασία Flavobacterium heparinum).[27] Αυτό το βακτήριο είναι ικανό να «χωνεύει» την ηπαρίνη (ή τη θειική ηπαράνη) ως τη μοναδική του πηγή άνθρακα και αζώτου. Για να το επιτύχει αυτό, παράγει σειρά ενζύμων όπως λυάσες, γλυκουρονιδάσες, σουλφοεστεράσες και σουλφαμιδάσες.[28] Σε μελέτες της ηπαρίνης έχουν κυρίως εφαρμογή οι λυάσες. Το βακτηρίδιο παράγει τρεις λυάσες της ηπαρίνης: τις ηπαρινάσες I (EC 4.2.2.7), II και III, καθεμιά από τις οποίες έχει ξεχωριστές ειδικότητες υποστρώματος[29][30], όπως φαίνεται στον πίνακα:
| Τύπος ηπαρινάσης | Υπόστρωμα |
| Ηπαρινάση I | GlcNS(±6S)-IdoA(2S) |
| Ηπαρινάση II | GlcNS/Ac(±6S)-IdoA(±2S) GlcNS/Ac(±6S)-GlcA |
| Ηπαρινάση III | GlcNS/Ac(±6S)-GlcA/IdoA (με προτίμηση για το GlcA) |

Το νιτρώδες οξύ μπορεί να χρησιμοποιηθεί για τον αποπολυμερισμό της ηπαρίνης (ή της θειικής ηπαράνης), σε pH ίσο με 1,5 ή 4. Σε αμφότερες τις συνθήκες, το νιτρώδες οξύ διαχωρίζει τα τμήματα της μοριακής αλυσίδας με απαμίνωση[31], ανάμεσα στους δεσμούς GlcNS-GlcA και GlcNS-IdoA, απλώς με λίγο αργότερο ρυθμό στο μεγαλύτερο (λιγότερο όξινο) pH. Η αντίδραση απαμινώσεως και άρα η διάσπαση της αλυσίδας είναι ανεξάρτητη της θειώσεως των μονοσακχαριδίων.
Στο πιο όξινο pH η απαμινωτική διάσπαση εκλύει ανόργανο SO4 και η GlcNS μετατρέπεται σε ανυδρομανόζη (aMan). Αυτή είναι μια πολύ καλή μέθοδος για να διακρίνουμε N-θειωμένους πολυσακχαρίτες, όπως η ηπαρίνη, από μη N-θειωμένους, όπως η θειική δερματάνη και η θειική χονδροϊτίνη, καθώς οι τελευταίοι δεν διασπώνται από το νιτρώδες οξύ.
Οι σημερινές κλινικές εργαστηριακές δοκιμές για την παρουσία ηπαρίνης στηρίζονται σε μία έμμεση μέτρηση της δράσεως του φαρμάκου, αντί σε άμεση μέτρηση της χημικής του παρουσίας. Αυτές περιλαμβάνουν τον ενεργοποιημένο μερικό χρόνο θρομβοπλαστίνης (APTT) και τη δράση του αντιπαράγοντα Xa. Το δείγμα επιλογής είναι συνήθως φρέσκο, πλάσμα αίματος.[32][33]
Η φαρμακευτικής ποιότητας ηπαρίνη λαμβάνεται από βλεννογόνους ιστούς ζώων που σφάζονται στα σφαγεία για το κρέας τους. Τέτοιοι ιστοί είναι τα χοιρινά εντόσθια και πνευμονικός ιστός βοοειδών.[34] Πρόοδοι στη συνθετική παραγωγή ηπαρίνης έχουν σημειωθεί το 2003 και το 2008.[35] Το 2011 αναφέρθηκε μια χημειοενζυματική διαδικασία συνθέσεως ηπαρινών μικρού μοριακού βάρους από απλά δισακχαρίδια.[36]
Η ηπαρίνη ανακαλύφθηκε το 1916 από τους Αμερικανούς Τζέυ Μακλήν (Jay McLean, 1890-1957) και Γουίλιαμ Χένρυ Χάουελ (William Henry Howell, 1860-1945), μολονότι κλινικές δοκιμές της άρχισαν μόλις το 1935.[37] Αρχικώς απομονώθηκε από κύτταρα συκωτιού (ήπατος) σκύλου, από όπου πήρε και το όνομά της.
Ο Μακλήν ήταν μόλις δευτεροετής φοιτητής της ιατρικής στο Πανεπιστήμιο Τζονς Χόπκινς και εργαζόταν υπό την επίβλεψη του Χάουελ ερευνώντας προθρομβωτικά παρασκευάσματα, όταν απομόνωσε ένα λιποδιαλυτό φωσφατούχο αντιθρομβωτικό σε ηπατικό ιστό σκύλου.[38] Το 1918 ο Χάουελ του έδωσε το όνομα «ηπαρίνη». Στις αρχές της δεκαετίας του 1920 ο Χάουελ απομόνωσε έναν υδατοδιαλυτό αντιθρομβωτικό πολυσακχαρίτη, που επίσης ονόμασε «ηπαρίνη», παρότι διαφορετικό.[39][40]
Μετά το 1930 αρκετοί ερευνητές άρχισαν να μελετούν την ηπαρίνη. Ο Erik Jorpes στο Ινστιτούτο Καρολίνσκα δημοσίευσε την έρευνά του επί της δομής της ηπαρίνης το 1935[41], κάτι που έδωσε τη δυνατότητα στη σουηδική εταιρεία Vitrum AB να δημιουργήσει το πρώτο προϊόν ηπαρίνης για ενδοφλέβια χρήση το 1936. Μεταξύ του 1933 και του 1936 τα Εργαστήρια Ιατρικών Ερευνών Connaught, τότε υπαγόμενα στο Πανεπιστήμιο του Τορόντο, τελειοποίησαν μια τεχνική για την παραγωγή ασφαλούς ηπαρίνης για ασθενείς. Οι πρώτες δοκιμές ηπαρίνης σε ανθρώπους άρχισαν τον Μάιο του 1935 και μέχρι το 1937 είχε γίνει συνείδηση ότι η ηπαρίνη των Connaught ήταν ένα ασφαλές, εύκολα διαθέσιμο και αποτελεσματικό αντιθρομβωτικό του αίματος. Μέχρι το 1933 η ηπαρίνη ήταν διαθέσιμη σε μικρές ποσότητες, ήταν εξαιρετικά ακριβή και τοξική, ώστε να μην έχει ιατρική αξία.[42]
Καθώς φαίνεται στον παρακάτω πίνακα, υπάρχουν αρκετές δυνατότητες για την ανάπτυξη της ηπαρίνης ή παρόμοιων μορίων ως φαρμάκων για πολλές διαφορετικές ασθένειες, πέρα από τη σημερινή αντιθρομβωτική χρήση.[43][44]
| Παθήσεις ευαίσθητες στην ηπαρίνη | Δράση της ηπαρίνης σε πειραματικές συνθήκες | Κλινικό στάδιο |
| AIDS | Μειώνει την ικανότητα προσροφήσεως του ιού HIV των τύπων 1 και 2 σε καλλιεργημένα κύτταρα T4.[45] | - |
| Σύνδρομο οξείας αναπνευστικής δυσχέρειας (ARDS) | Μειώνει την ενεργοποίηση των κυττάρων και τη συσσώρευσή τους στους αεραγωγούς, εξουδετερώνει κυτοτοξικά κυτταρικά προϊόντα και βελτιώνει την πνευμονική λειτουργία σε πειραματόζωα. | Ελεγχόμενες κλινικές δοκιμές |
| Αλλεργική εγκεφαλομυελίτιδα | Αποτελεσματικό σε πειραματόζωα | - |
| Αλλεργική ρινίτιδα | Παρόμοια με τη δράση στην περίπτωση του ARDS, αν και δεν έχει ελεγχθεί συγκεκριμένο ρινικό μοντέλο. | Ελεγχόμενες κλινικές δοκιμές |
| Αρθρίτιδα | Παρεμποδίζει τη συσσώρευση κυττάρων, την καταστροφή του κολλαγόνου και την αγγειογένεση. | Μη δημοσιευμένη αναφορά |
| Άσθμα | Παρόμοια με τη δράση στην περίπτωση του ARDS, ενώ έχει αποδειχθεί και ότι βελτιώνει την πνευμονική λειτουργία σε πειραματόζωα. | Ελεγχόμενες κλινικές δοκιμές |
| Καρκίνος | Παρεμποδίζει την αύξηση όγκων, τις μεταστάσεις και την αγγειογένεση. Αυξάνει τον χρόνο επιβιώσεως σε πειραματόζωα. | Αρκετές μη δημοσιευμένες αναφορές |
| Αντιδράσεις υπερευαισθησίας (delayed-type) | Αποτελεσματικό σε πειραματόζωα | - |
| Ιδιοπαθής φλεγμονώδης εντερική νόσος | Παρεμποδίζει τη μεταφορά φλεγμονωδών κυττάρων γενικώς. | Controlled clinical trials |
| Διάμεση κυστίτιδα | Αποτελεσματική σε άνθρωπο | Παρόμοιο μόριο χρησιμοποιείται τώρα κλινικά |
| Απόρριψη μοσχεύματος | Παρατείνει την επιβίωση ετερομοσχευμάτων σε πειραματόζωα. | - |
Ως αποτέλεσμα της δράσεως της ηπαρίνης σε τόσο ευρεία ποικιλία παθήσεων, ένας αριθμός φαρμάκων με μοριακές δομές ταυτόσημες ή πολύ παρόμοιες με αυτές μερών της πολυμερικής αλυσίδας της ηπαρίνης βρίσκονται ήδη σε ανάπτυξη.[43]
| Μόριο | Ιδιότητες σε σχέση με την ηπαρίνη | Βιολογική δράση |
| Τετρασακχαρίτης ηπαρίνης | Μη αντιθρομβωτικό, λήψη από το στόμα | Αντιαλλεργικό |
| Πολυθειική πεντοζάνη | Φυτικής προελεύσεως, μικρή αντιθρομβωτική δράση, αντιφλεγμονώδες, λήψη από το στόμα | Αντιφλεγμονώδες, αντικολλητικό, αντιμεταστατικό |
| Θειική φωσφομανοπεντανόζη | Ισχυρός αναστολέας της δράσεως του ενζύμου ηπαρανάση | Αντιμεταστατικό, αντιαγγειογενετικό, αντιφλεγμονώδες |
| Επιλεκτικά O-αποθειωμένη ηπαρίνη | Μη αντιθρομβωτικό | Αντιφλεγμονώδες, αντιαλλεργικό |
Εκτός από τον ιστό βοοειδών και χοίρων από τους οποίους λαμβάνεται συνήθως η φαρμακευτικής ποιότητας ηπαρίνη, έχει επίσης ληφθεί και χαρακτηρισθεί από τα εξής ζωικά είδη:
Η βιολογική λειτουργία της ηπαρίνης στα εκ των ανωτέρω είδη 6 ως 11 δεν είναι ξεκάθαρη και υποστηρίζει την άποψη ότι ο κύριος φυσιολογικός ρόλος της ηπαρίνης στο ζωικό βασίλειο γενικώς δεν είναι ο αντιθρομβωτικός. Αυτά τα είδη δεν διαθέτουν κάποιο σύστημα θρομβώσεως του αίματος παρόμοιο με αυτό των ειδών 1 ως 5. Ο παραπάνω κατάλογος δείχνει επίσης το πόσο η ηπαρίνη έχει διατηρηθεί κατά την εξέλιξη των ειδών, με μόρια παρόμοιας δομής να παράγονται από μία ευρεία ποικιλία οργανισμών, που ανήκουν σε διαφορετικές συνομοταξίες.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.