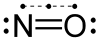Μονοξείδιο του αζώτου
Το νιτρικό οξείδιο ή μονοξείδιο του αζώτου,[3] είναι μια μοριακή, χημική ένωση με μοριακό τύπο of ·NO. / From Wikipedia, the free encyclopedia
Το νιτρικό οξείδιο (Nitric oxide) ή μονοξείδιο του αζώτου ( nitrogen monoxide),[2] είναι μια μοριακή, χημική ένωση με μοριακό τύπο of ·NO. Ένα από τα κύρια οξείδια του αζώτου, είναι άχρωμο αέριο σε πρότυπες συνθήκες. Το μονοξείδιο του αζώτου είναι ελεύθερη χημική ρίζα—δηλαδή, η δεσμική δομή του (bonding structure) περιλαμβάνει περιλαμβάνει ένα ασύζευκτο ηλεκτρόνιο (unpaired electron),[3] που παριστάνεται με τελεία (·) στο άτομο του αζώτου—και είναι στην κατηγορία των ετεροπυρηνικών διατομικών μορίων που έχουν ιστορικό θεωρητικό ενδιαφέρον (για τις ιδέες που έδωσε στη διαμόρφωση των πρώιμων σύγχρονων θεωριών των δεσμών). Είναι ένα ιδιαίτερα σημαντικό ενδιάμεσο προϊόν στη χημική βιομηχανία. Επιπλέον, κάποια ποσότητα παράγεται αναπόφευκτα κατά την καύση των ορυκτών καυσίμων στα εργοστάσια ηλεκτρικής ενέργειας και στους κινητήρες αυτοκινήτων, με το μεγαλύτερο μέρος να δημιουργείται όταν υπάρχει περισσότερος αέρας ή υψηλότερες θερμοκρασίες από ό,τι απαιτείται για αποτελεσματική και πλήρη καύση του καυσίμου. Παράγεται επίσης στη φύση από τις ακραίες υψηλές θερμοκρασίες του αέρα που παράγονται κατά μήκος της διαδρομής των κεραυνών στις καταιγίδες.
 | |||
| |||
| Ονόματα | |||
|---|---|---|---|
| ΟνοματολογίαIUPAC
Νιτρικό οξείδιο | |||
| ΆλλαΟνόματα
Μονοξείδιο του αζώτου Οξείδιο του αζώτου (ΙΙ) | |||
| Αναγνωριστικά | |||
| 10102-43-9 | |||
| 3DMet | B00122 | ||
| ChEBI | CHEBI:16480 | ||
| ChEMBL | ChEMBL1200689 | ||
| ChemSpider | 127983 | ||
| DrugBank | DB00435 | ||
| Αριθμός_EC | 233-271-0 | ||
| 451 | |||
InChI=1S/NO/c1-2 Key: MWUXSHHQAYIFBG-UHFFFAOYSA-N InChI=1/NO/c1-2 Key: MWUXSHHQAYIFBG-UHFFFAOYAI | |||
IUPHAR/BPS |
|||
| Jmol 3Δ Πρότυπο | Image | ||
| KEGG | D00074 | ||
| PubChem | 145068 | ||
| Αριθμός RTECS | QX0525000 | ||
[N]=O | |||
| UNII | 31C4KY9ESH | ||
| Αριθμός UN | 1660 | ||
| Ιδιότητες | |||
| NO | |||
| Μοριακή μάζα | 30,01 g·mol−1 | ||
| Εμφάνιση | Άχρωμο αέριο | ||
| Πυκνότητα | 1,3402 g dm−3 | ||
| Σημείο τήξης | −164 °C (−263 °F; 109 K) | ||
| Σημείο βρασμού | −152 °C (−242 °F; 121 K) | ||
| Διαλυτότητα στο νερό | 0,0098 g/100ml (0 °C) 0,0056 g/100ml (20 °C) | ||
Δείκτης διάθλασης (nD) |
1,0002697 | ||
| Δομή | |||
| γραμμικό (ομάδα σημείων C∞v) | |||
| Θερμοχημεία | |||
Πρότυπη μοριακή εντροπία (S |
210,76 J K−1 mol−1 | ||
Πρότυπη ενθαλπία σχηματισμού (ΔfH |
91,29 kJ mol−1 | ||
| Φαρμακολογία | |||
| Κωδικοί ATC | R07AX01 | ||
| Φαρμακοκινητική: | |||
| μέσω πνευμονικού τριχοειδούς στρώματος | |||
Βιολογική ημιζωή |
2–6 δευτερόλεπτα | ||
| Κίνδυνοι | |||
| Δελτίο δεδομένων ασφάλειας | External MSDS | ||
Ταξινόμηση EΕ (DSD) |
|||
| Φράσεις-R | R8, R23, R34, R44 | ||
| Φράσεις-S | S1, S17, S23, S36/37/39, S45 | ||
| NFPA 704 | |||
| Θανάσιμη δόση ή συγκέντρωση (LD, LC): | |||
LC50 (μέση θανατηφόρα συγκέντρωση) |
315 ppm (κουνέλι, 15 min) 854 ppm (επίμυς, 4 hr) 320 ppm (ποντίκι)[1] | ||
| 2500 ppm (ποντίκι, 12 min)[1] | |||
| Σχετικές ενώσεις | |||
| Πεντοξείδιο του διαζώτου Τετροξείδιο του διαζώτου | |||
Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες (25°C, 100 kPa). | |||
| | |||
| Infobox references | |||
Στα θηλαστικά, συμπεριλαμβανομένων των ανθρώπων, το μονοξείδιο του αζώτου είναι ένα σημαντικό κυτταρικό σηματοδοτικό μόριο (signaling molecule) που εμπλέκεται σε πολλές φυσιολογικές και παθολογικές διεργασίες.[4] Είναι ένα ισχυρό αγγειοδιασταλτικό με μικρό χρόνο ημιζωής μερικών δευτερολέπτων στο αίμα. Γνωστά από παλιά φαρμακευτικά σκευάσματα όπως η νιτρογλυκερίνη και το νιτρώδες αμύλιο (amyl nitrite) βρέθηκαν να είναι πρόδρομες ενώσεις στο μονοξείδιο του αζώτου περισσότερο από έναν αιώνα μετά την πρώτη τους χρήση στην ιατρική. Χαμηλά επίπεδα μονοξειδίου του αζώτου είναι σημαντικά στην προστασία οργάνων όπως το ήπαρ από ισχαιμική βλάβη (ischemic damage). Η παραγωγή μονοξειδίου του αζώτου σχετίζεται με τη μη αλκοολική λιπώδη νόσο του ήπατος (nonalcoholic fatty liver disease ή NAFLD) και είναι βασική για τον ηπατικό λιπιδικό μεταβολισμό σε περίπτωση ασιτίας.[5]
Ως συνέπεια της σημασίας του στη νευροεπιστήμη, τη φυσιολογία και την ανοσολογία (immunology), το μονοξείδιο του αζώτου ανακηρύχθηκε "Μόριο του έτους" το 1992.[6] Η αναζήτηση για τις λειτουργίες του οδήγησε στο βραβείο Νόμπελ 1998 για την ανακάλυψη του ρόλου του μονοξειδίου του αζώτου ως καρδειοαγγειακό μόριο σηματοδότησης. Το μονοξείδιο του αζώτου δεν πρέπει να συγχέεται με το υποξείδιο του αζώτου (N2O), ένα αναισθητικό, ή με το διοξείδιο του αζώτου (NO2), ένα καφετή τοξικό αέριο και σημαντικός ατμοσφαιρικός ρύπος που είναι ένα προϊόν στο οποίο οξειδώνεται ταχύτητα στον αέρα το μονοξείδιο του αζώτου.
Ταξινομείται ως πολύ επικίνδυνη ουσία στις ΗΠΑ όπως ορίζεται στην ενότητα 302 του Emergency Planning and Community Right-to-Know Act (42 U.S.C. 11002) και υπόκειται σε αυστηρή αναφορά απαιτήσεων από εγκαταστάσεις που παράγουν, αποθηκεύουν, ή το χρησιμοποιούν σε σημαντικές ποσότητες.[7]