Amonia karbonato
kemia kombinaĵo From Wikipedia, the free encyclopedia
Remove ads
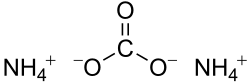
Diamonia trioksokarbonato[4] aŭ (NH4)2CO3 estas kemia substanco rezultanta el la reakcio inter la amonia hidroksido kaj la karbonata acido. Kiam varmigita, ĝi facile malkomponiĝas kiel amoniako kaj karbona duoksido, kaj uzatas kiel fermentigagento kaj ankaŭ kiel flarsalo okaze de konsciencoperdo. Ĝi estas konata kiel bakista amoniako kaj estas antaŭanto de la plej modernaj fermentigaj agentoj samkiel natria karbonato kaj natria bikarbonato.
| Amonia karbonato | ||
 | ||
 | ||
 | ||
| Alternativa(j) nomo(j) | ||
| Salo de Hartshorn[1] Bakeja fermento Ammoniæ carbonas[2]
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 506-87-6 | |
| ChemSpider kodo | 10048 | |
| PubChem-kodo | 10480 | |
| Fizikaj proprecoj | ||
| Aspekto | Blanka pulvoro kun amoniakodoro | |
| Molmaso | 96.09 g mol−1 | |
| Smiles | O=C(O)O.N.N | |
| Denseco | 1.50 g/cm3 (likva) | |
| Fandopunkto | 58 °C (136 ℉; 331 K) | |
| Bolpunkto | Malkomponiĝas | |
| Solvebleco:Akvo | Tute solvebla, malkomponiĝas en varma akvo | |
| Mortiga dozo (LD50) | 1975 mg/Kg (muso, buŝa) | |
| Sekurecaj Indikoj | ||
| Risko | R22 R36 | |
| Sekureco | S24 S25 | |
| Pridanĝeraj indikoj | ||
| Danĝero | ||
| GHS etikedigo de kemiaĵoj | ||
| GHS Damaĝo-piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H302 | |
| GHS Deklaroj pri antaŭgardoj | P101, P102, P103, P264, P270, P301, P310, P301+312, P330, P353[3] | |
(25 °C kaj 100 kPa) | ||
Remove ads
Proprecoj
Ĝi ne estas facile preparebla en ties pura formo. Komercaj produktoj ĝenerale estas miksaĵo da "amonia karbamato" kaj "amonia bikarbonato". Tamen, la plej ordinara maniero estas per kontakto de la karbona duoksido en amoniaka solvaĵo. Ĉirkaŭ 7 mil tunoj/jare estis produktitaj ĝis 1997. Amonia karbonato estas neakordigebla kun acidoj, kiuj malkomponas ĝin, estigante amoniajn salojn kaj liberigante karbonan duoksidon. Ĝi precipitas la karbonaton aŭ la hidroksidon de plejmulto el la metaloj kaj la nesolveblaj alkaloj el la solvaĵoj kun ties saloj.
Amonia karbonato larĝe malkomponiĝas kiam dissolvita en akvo; ĝiaj solvaĵoj estas iritaj al la mukozaj membranoj dum liberigo de amonio. Per inhalado ĝi uzatas en solvaĵoj kiel stimulilo en kazoj de sinkopo, spirmanko kaj kiel likviga ekspektorigilo en kazoj de bronkito.
Remove ads
Literaturo
- Concise Encyclopedia Chemistry, Mary Eagleson
- The Facts on File Chemistry Handbook, Diagram Group
- Inorganic Chemistry, Egon Wiberg, Nils Wiberg
- The Chemical Company Arkivigite je 2015-07-07 per la retarkivo Wayback Machine
- Sigma Aldrich
Vidu ankaŭ
Referencoj
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads


