
Electrón de valencia
De Wikipedia, la enciclopedia encyclopedia
Los electrones de valencia son los electrones que se encuentran en el nivel principal de energía (n)[1] más alto del átomo,[2] siendo estos los responsables de la interacción entre átomos de distintas especies o entre los átomos de una misma. Los electrones en los niveles de energía externos son aquellos que serán utilizados en la formación de compuestos y a los cuales se les denomina como electrones de valencia.
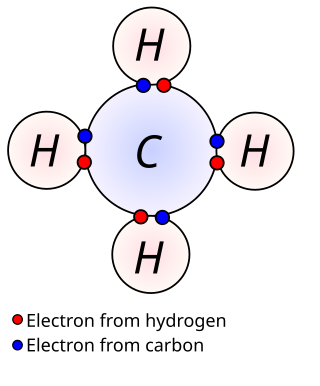
Estos electrones son los que presentan la facilidad de formar enlaces.[3] Estos enlaces pueden darse de diferente manera, ya sea por intercambio de estos electrones, por compartición de pares entre los átomos en cuestión o por el tipo de interacción que se presenta en el enlace metálico, que consiste en un "traslape" de bandas. Según sea el número de estos electrones, será el número de enlaces que puede formar cada átomo con otro u otros.
Solo los electrones externos de un átomo pueden ser atraídos por otro átomo cercano. Por lo general, los electrones del interior son afectados en menor medida y tampoco los electrones en las subcapas d llenas y en las f, porque están en el interior del átomo y no en la superficie.
La valencia de un elemento es el número de electrones que necesita o que le sobra para tener completo su último nivel. La valencia de los gases nobles, por tanto, será cero, ya que tienen completo el último nivel. En el caso del sodio, la valencia es 1, ya que tiene un solo electrón de valencia, si pierde un electrón se queda con el último nivel completo.
Un átomo con una cáscara cerrada de electrones de valencia (correspondiente a una configuración de gas noble) tiende a ser químicamente inerte. Los átomos con uno o dos electrones de valencia más de una cáscara cerrada son altamente reactivos debido a la relativamente baja energía para eliminar los electrones de valencia adicionales para formar un ion positivo. Un átomo con uno o dos electrones menos que una capa cerrada es reactivo debido a su tendencia a ganar los electrones de valencia que le faltan y formar un ion negativo, o bien a compartir electrones de valencia y formar un enlace covalente.
Al igual que un electrón interno, un electrón de valencia tiene la capacidad de absorber o liberar energía en forma de fotón. Una ganancia de energía puede provocar que el electrón se mueva (salte) a una capa exterior; esto se conoce como excitación atómica. O el electrón puede incluso liberarse de la envoltura de su átomo asociado; esto es ionización para formar un ion positivo. Cuando un electrón pierde energía (provocando así la emisión de un fotón), puede desplazarse a una capa interna que no esté totalmente ocupada.