Top Qs
Línea de tiempo
Chat
Contexto
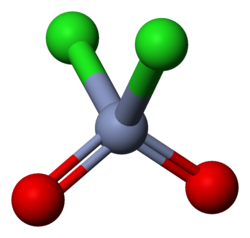
Cloruro de cromilo
compuesto químico De Wikipedia, la enciclopedia libre
Remove ads
El cloruro de cromilo es un compuesto inorgánico cuya fórmula es CrO2Cl2. Se trata de un compuesto de color marrón rojizo que a temperatura ambiente es un líquido volátil, algo poco habitual en los metales de transición.
Remove ads
Preparación
El cloruro de cromilo puede prepararse haciendo reaccionar cromato de potasio o dicromato de potasio con cloruro de hidrógeno al que se añade ácido sulfúrico, y a continuación se destila.[3][4]
K2Cr2O7 + 6 HCl → 2 CrO2Cl2 + 2 KCl + 3 H2O
El ácido sulfúrico hace las veces de un agente deshidratante. También se puede preparar de forma directa al exponer trióxido de cromo al cloruro de hidrógeno anhidro en estado gaseoso.
CrO3 + 2 HCl ⇌ CrO2Cl2 + H2O
El método usado para preparar el cloruro de cromilo es la base de una comprobación cualitativa del cloruro: se calienta una muestra que se sospecha que contiene cloruro con una mezcla de dicromato potásico y ácido sulfúrico concentrado. Si hay cloruro, se forma cloruro de cromilo, visible por los vapores rojos que desprende el CrO2Cl2. No se forman compuestos análogos con fluoruros, bromuros, yoduros y cianuros.
Remove ads
Reactivo para la oxidación de alquenos
El cloruro de cromilo oxida a los alquenos internos y los convierte en alfa-clorocetonas o derivados relacionados.[5] También ataca a los grupos metilo-bencílicos para formar aldehídos mediante la oxidación de Étard. El diclorometano es un disolvente idóneo para este tipo de reacciones.[6]
Consideraciones de seguridad

El CrO2Cl2 se descompone de forma «violenta» en contacto con el agua para liberar ácido clorhídrico (HCl) y ácido crómico (H2CrO4). Aunque no es combustible, el cloruro de cromilo es un oxidante fuerte y puede inflamarse de forma espontánea o explotar si entra en contacto con sustancias inflamables. En caso de incendio, no se debe entrar en contacto directo con el agua.
Además, el cloruro de cromilo es muy corrosivo y quema fácilmente la piel y los ojos, y su ingestión provocaría daños internos graves. Sus vapores también son muy irritantes para cualquier parte del cuerpo.[7]
Crónico: El CrVI puede producir anomalías cromosómicas y es un carcinógeno humano a través de la vía respiratoria.[8] Una exposición prolongada al cloruro de cromilo puede provocar úlceras en la piel.[7]
Véase también
Referencias
Enlaces externos
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads