Top Qs
Línea de tiempo
Chat
Contexto
Sulfato de zinc
compuesto químico De Wikipedia, la enciclopedia libre
Remove ads
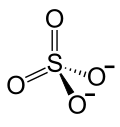
El sulfato de zinc, también conocido como sulfato de cinc, vitriolo blanco, vitriolo de Goslar, Goslarita o caparrosa blanca, es un compuesto químico cristalino, incoloro y soluble en agua, de fórmula ZnSO4, aunque siempre va acompañado de un determinado número de moléculas de agua de hidratación.
Remove ads
Formas hidratadas y anhidra
Suele presentarse como sal heptahidratada, ZnSO4·7H2O. A 30 °C pierde una molécula de agua y se transforma en ZnSO4·6H2O.[3] A 70 °C pierde otras cinco moléculas de agua y se transforma en ZnSO4·H2O. Finalmente, a 280 °C pierde la última molécula de agua y se transforma en la sal anhidra.[4]
Obtención
Resumir
Contexto
En la Naturaleza se presenta formando parte del mineral goslarita (heptahidrato), conocido también como "vitriolo blanco" y de la bianchita (hexahidrato). Puede prepararse por reacción de zinc o del óxido de zinc con ácido sulfúrico en disolución acuosa.
O por oxidación enérgica del sulfuro de zinc, componente de la blenda.
- .
También puede prepararse añadiendo zinc sólido a disoluciones de sulfato de cobre (II) o sulfato de hierro (II).
- .
- .
Remove ads
Usos
Se usa como suplemento de zinc en la alimentación animal, para preparar abonos y sprays agrícolas. ZnSO4·7H2O se usa en fabricación de litopón (blanco de zinc), y rayón (seda artificial), como conservante de madera, como electrolitos para plateado con zinc (zincado), como mordiente de coloración, para preservar pieles y cuero, y en Medicina, como astringente y emético.
Una disolución acuosa de sulfato de zinc resulta efectiva para eliminar musgo de los pavimentos y suelos. [5]
Se han referido usos del sulfato de zinc para enmascarar las pruebas y análisis antidroga porque actúa como quelante de las moléculas, retirándolas de la orina.[6]
Referencias
Enlaces externos
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads