
Ácido acético
compuesto químico / De Wikipedia, la enciclopedia encyclopedia
Estimado Wikiwand AI, Seamos breves simplemente respondiendo estas preguntas clave:
¿Puede enumerar los principales datos y estadísticas sobre Ácido acético?
Resumir este artículo para un niño de 10 años
El ácido acético (también llamado ácido metilcarboxílico o ácido etanoico) puede encontrarse en forma de ion acetato. Se encuentra en el vinagre, y es el principal responsable de su sabor y olor agrios. Su fórmula es CH3-COOH (C2H4O2). De acuerdo con la IUPAC, se denomina sistemáticamente ácido etanoico.
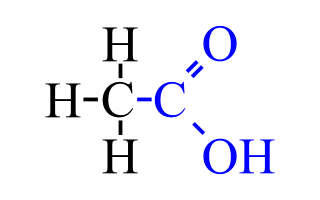
 Estructura plana del ácido acético | ||
 Estructura tridimensional del ácido acético | ||
| Nombre IUPAC | ||
| ácido etanoico | ||
| General | ||
| Otros nombres | Ácido acético | |
| Fórmula semidesarrollada | CH3COOH | |
| Fórmula molecular | C2H4O2 | |
| Identificadores | ||
| Número CAS | 64-19-7[1] | |
| Número RTECS | AF1225000 | |
| ChEBI | 15366 | |
| ChEMBL | CHEMBL539 | |
| ChemSpider | 171 | |
| DrugBank | DB03166 | |
| PubChem | 176 | |
| UNII | Q40Q9N063P | |
| KEGG | D00010 | |
|
CC(O)=O
| ||
| Propiedades físicas | ||
| Apariencia | cristales | |
| Densidad | 1049 kg/m³; 1,049 g/cm³ | |
| Masa molar | 60 021 129 372 g/mol | |
| Punto de fusión | 290 K (17 °C) | |
| Punto de ebullición | 391,2 K (118 °C) | |
| Propiedades químicas | ||
| Acidez | 4,74 pKa | |
| Momento dipolar | 1,74 D | |
| Peligrosidad | ||
| SGA |
  | |
| NFPA 704 |
2
3
0
| |
| Frases H | H226, H314 | |
| Frases P | P280, P305+P351+P338, P310 | |
| Riesgos | ||
| Ingestión | Dolor de garganta, vómito, diarrea, dolor abdominal, sensación de quemazón en el tracto digestivo. | |
| Inhalación | Dolor de garganta, dificultad respiratoria, tos. | |
| Piel | Quemadura. | |
| Ojos | Irritación, visión borrosa, quemaduras profundas. | |
| Compuestos relacionados | ||
| Ácidos relacionados |
Ácido metanoico Ácido propílico Ácido butírico | |
| Compuestos relacionados |
Acetamida Acetato de etilo, Anhidrido acético, Acetonitrilo, Acetaldehído, Etanol, Cloruro de etanoilo | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Es el segundo ácido carboxílico más simple después del ácido fórmico o metanoico, que solo tiene un carbono, y antes del ácido propanoico, que ya tiene una cadena de tres carbonos.
El punto de fusión es 16,6 °C y el punto de ebullición es 117,9 °C. Es un líquido o cristal incoloro con sabor a ácido, vinagre, uno de los ácidos nucleicos más simples y un reactivo químico ampliamente utilizado.[2]
En disolución acuosa, puede perder el protón del grupo carboxilo para dar su base conjugada, el acetato. Su pKa es de 4,8 a 25 °C, lo cual significa, que al pH moderadamente ácido de 4,8, la mitad de sus moléculas se habrán desprendido del protón. Esto hace que sea un ácido débil y que, en concentraciones adecuadas, pueda formar disoluciones tampón con su base conjugada. La constante de disociación a 20 °C es Ka = 1,75·10−5.
Es de interés para la química orgánica como reactivo, para la química inorgánica como ligando, y para la bioquímica como metabolito (activado como acetil-coenzima A). También se utiliza como sustrato, en su forma activada, en reacciones catalizadas por las enzimas conocidas como acetiltransferasas y, en concreto, histona acetiltransferasas.
Hoy día, la vía natural de su obtención es a través de la carbonilación (reacción con CO) de metanol. Antaño se producía por oxidación de etileno en acetaldehído, el cual se oxidaba posteriormente para obtener, finalmente, el ácido acético.
