
Ácido sulfhídrico
compuesto químico / De Wikipedia, la enciclopedia encyclopedia
Estimado Wikiwand AI, Seamos breves simplemente respondiendo estas preguntas clave:
¿Puede enumerar los principales datos y estadísticas sobre Ácido sulfhídrico?
Resumir este artículo para un niño de 10 años
El ácido sulfhídrico en disolución acuosa (H2S(aq)), es un hidrácido de fórmula H2S. Este gas, más pesado que el aire, es inflamable, incoloro, tóxico, odorífero: su olor es el de materia orgánica en descomposición, similar al olor de los huevos podridos. A pesar de ello, en el organismo humano desempeña funciones esenciales.
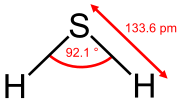 Geometría del sulfuro de hidrógeno. | ||
 | ||
| Nombre IUPAC | ||
| Sulfuro de hidrógeno | ||
| General | ||
| Otros nombres | ácido sulfhídrico (aq) | |
| Fórmula semidesarrollada | HSH | |
| Fórmula estructural |
 | |
| Fórmula molecular | H2S | |
| Identificadores | ||
| Número CAS | [7783-06-4][1] | |
| Número RTECS | MX1225000 | |
| ChEBI | 16136 | |
| ChEMBL | CHEMBL1200739 | |
| ChemSpider | 391 | |
| PubChem | 402 | |
| UNII | YY9FVM7NSN | |
| KEGG | C00283 | |
| Propiedades físicas | ||
| Apariencia | gas incoloro | |
| Masa molar | 34,1 g/mol | |
| Punto de fusión | 187 K (−86 °C) | |
| Punto de ebullición | 213 K (−60 °C) | |
| Propiedades químicas | ||
| Acidez | 6,89 pKa | |
| Solubilidad en agua | 0,33 | |
| Momento dipolar | 0,97 D | |
| Termoquímica | ||
| ΔfH0gas | -20,5 kJ/mol | |
| S0gas, 1 bar | 205,77 J·mol–1·K | |
| Peligrosidad | ||
| Punto de inflamabilidad | 190,6 K (−83 °C) | |
| NFPA 704 |
4
4
0
| |
| Frases R | R12, R26, R50 | |
| Frases S | (S1/2), S9, S16, S36, S38, S45, S61 | |
| Riesgos | ||
| Ingestión | puede causar náuseas y vómitos. | |
| Inhalación | peligroso; puede ser fatal. | |
| Piel | puede causar picazón y dolor. | |
| Ojos | puede causar quemaduras. | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
En la nomenclatura química la desinencia -uro corresponde a los haluros, es decir, a las sales que no contienen oxígeno. Puesto que sal "es un compuesto iónico formado por un catión distinto de H+ y un anión distinto de OH- u O2-: ácido + base --> sal + agua",[2] la expresión «sulfuro de hidrógeno» resulta extraña, pues implica que el hidrógeno se sustituye a sí mismo.
Para evitar esta incongruencia en su denominación, al H2S se le podría considerar como disolución acuosa (aq en la fórmula), es decir ácido sulfhídrico.
Con bases fuertes genera sales: los sulfuros. Su punto de ebullición es de 212,86 K. El ácido sulfhídrico se mantiene unidos gracias a enlaces
