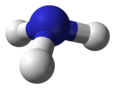
آمونیاک
ترکیبی از گازهای نیتروژن (N²) و هیدروژن(H²) است / From Wikipedia, the free encyclopedia
آمونیاک (به انگلیسی: Ammonia) با فرمول شیمیایی NH3، ترکیبی از نیتروژن و هیدروژن است. آمونیاک یک هیدرید دوتایی پایدار و سادهترین هیدرید آن، یک گاز بیرنگ با بوی تند مشخص است. آمونیاک یک زباله نیتروژنی متداول است، بهویژه در میان موجودات آبزی، و با عملکرد به عنوان یک پیش مادهٔ غذایی و در کودها بهطور قابل توجهی به نیازهای غذایی موجودات زنده در زمین کمک میکند. آمونیاک، بهطور مستقیم یا غیرمستقیم، همچنین یکی از عناصر سازنده بسیاری از محصولات دارویی است و در بسیاری از محصولات تمیز کنندهٔ تجاری مورد استفاده قرار میگیرد. این ماده عمدتاً با جابجایی هوا و آب به سمت پایینتر جمع میشود.
| آمونیاک | |||
|---|---|---|---|
| |||
Azane | |||
دیگر نامها Hydrogen nitride | |||
| شناساگرها | |||
| شماره ثبت سیایاس | ۷۶۶۴-۴۱-۷ | ||
| پابکم | ۲۲۲ | ||
| UNII | 5138Q19F1X | ||
| شمارهٔ ئیسی | 231-635-3 | ||
| شمارهٔ یواِن | 1005 | ||
| KEGG | D02916 | ||
| MeSH | Ammonia | ||
| ChEBI | CHEBI:16134 | ||
| ChEMBL | CHEMBL۱۱۶۰۸۱۹ | ||
| شمارهٔ آرتیئیسیاس | BO0875000 | ||
مرجع بیلشتین |
3587154 | ||
مرجع جیملین |
79 | ||
| 3DMet | B00004 | ||
| جیمول-تصاویر سه بعدی | Image 1 | ||
| |||
| |||
| خصوصیات | |||
| فرمول مولکولی | NH3 | ||
| جرم مولی | 17.031 g/mol | ||
| شکل ظاهری | Colourless gas with strong pungent odour | ||
| چگالی | 0.86 kg/m3 (1.013 bar at boiling point) 0.73 kg/m3 (1.013 bar at 15 °C) 681.9 kg/m3 at -33.3 °C (liquid)[1] 817 kg/m3 at -80 °C (transparent solid)[2] | ||
| دمای ذوب | −۷۷٫۷۳ درجه سلسیوس (−۱۰۷٫۹۱ درجه فارنهایت؛ ۱۹۵٫۴۲ کلوین) | ||
| دمای جوش | −۳۳٫۳۴ درجه سلسیوس (−۲۸٫۰۱ درجه فارنهایت؛ ۲۳۹٫۸۱ کلوین) | ||
| انحلالپذیری در آب | 47% (0 °C) 31% (25 °C) 28% (50 °C)[3] | ||
| اسیدی (pKa) | 32.5 (-33 °C)[4] 10.5 (DMSO) | ||
| خاصیت بازی (pKb) | 4.75 | ||
| ساختار | |||
| شکل مولکولی | Trigonal pyramid | ||
| گشتاور دوقطبی | 1.42 D | ||
| خطرات | |||
| GHS pictograms |     [5] [5] | ||
| GHS hazard statements | H221, H280, H314, H331, H400[5] | ||
| GHS precautionary statements | P210, P261, P273, P280, P305+351+338, P310[5] | ||
| شاخص ئییو | 007-001-00-5 (anhydrous) 007-001-01-2 (solutions) | ||
| طبقهبندی ئییو | Toxic (T) Corrosive (C) Dangerous for the environment (N) | ||
| کدهای ایمنی | R۱۰, R۲۳, R۳۴, R50 | ||
| شمارههای نگهداری | (S1/2), S۹, S۱۶, S26, S36/37/39, S45, S61 | ||
| لوزی آتش | imagemap_invalid_title | ||
| نقطه اشتعال | |||
| دمای خودآتشگیری | |||
| محدودیتهای انفجار | ۱۵–۲۸٪ | ||
| آمریکا Permissible exposure limit (PEL) |
50 ppm (25 ppm ACGIH - TLV; 35 ppm STEL) | ||
| ترکیبات مرتبط | |||
| دیگر کاتیونها | فسفین آرسین Stibine | ||
| مرتبط با nitrogen hydrides | هیدرازین هیدرازوئیک اسید | ||
| ترکیبات مرتبط | هیدروکسید آمونیوم | ||
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |||
| | |||
| Infobox references | |||
|
| |||
هرچند که در طبیعت - چه زمینی و چه در سیارههای بیرونی منظومه شمسی - استفادهٔ گسترده از آن متداول است، اما آمونیاک به شکل غلیظ خود بسیار خورنده و خطرناک است. در ایالات متحده این ماده به عنوان مادهای بسیار خطرناک طبقهبندی میشود و در مراکز تولید، ذخیره یا استفاده در مقادیر قابل توجه نیازمند گزارش و سختگیری است.[6]
تولید جهانی صنعتی آمونیاک در سال ۲۰۲۰ نزدیک به ۱۸۰ میلیون تن بود،[7] آمونیاک صنعتی یا به صورت آمونیوم هیدروکسید (معمولاً ۲۸٪ آمونیاک در آب) یا به صورت آمونیاک مایع فشرده بیآب یا یخچالدار که در اتومبیلهای با مخزن ویژه یا در سیلندر حمل و عرضه میشود.[8] بازار جهانی آمونیاک در سال ۲۰۱۶ معادل ۶۵٫۴۸ میلیارد دلار ارزیابی شدهاست. پیشبینی میشود این صنعت تا سال ۲۰۲۵ به ۷۶٫۶۴ میلیارد دلار برسد.[9]
در طبیعت از تجزیهٔ مواد آلی ازت دار همچون اوره ادرار بهدست میآید.
رومیهای باستان آمونیوم کلرید را به عنوان پول و سپرده استفاده میکردند. آنها سنگ آمونیوم را از مکانی به نام پرستشگاه ژوپیتر یا همان لیبی جدید جمعآوری میکردند. اما آمونیاک به شکل نمک آمونیاک نخستین بار توسط جابر ابن حیان در قرن ۷ شناخته شد.[10]