Top Qs
Chronologie
Chat
Contexte
Chlorure de molybdène(V)
composé chimique De Wikipédia, l'encyclopédie libre
Remove ads
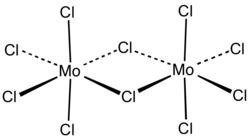
Le chlorure de molybdène(V), ou pentachlorure de molybdène, est un composé chimique de formule (MoCl5)2. Il se présente sous la forme d'un solide bleu-noir ininflammable très hygroscopique paramagnétique à l'odeur piquante et qui réagit violemment au contact de l'eau. Sa couleur peut virer au vert foncé s'il développe des oxychlorures. Sa molécule à l'état solide est un dimère, qui se dissocie en monomères à l'état gazeux, où il prend une teinte rouge[4].
Remove ads
Structure et propriétés
Le pentachlorure de molybdène cristallise dans une forme α du système monoclinique selon le groupe d'espace C/2m (no 12) avec comme paramètres cristallins a = 1 731 pm, b = 1 781 pm, c = 607,9 pm et β = 95,7°[5], soit une structure cristalline distincte de celle du NbCl5. On en connaît également trois autres polymorphes : la forme β a une structure cristalline triclinique avec le groupe d'espace P1 (no 2), la forme γ a une structure cristalline orthorhombique avec le groupe d'espace Pnma (no 62) et la forme δ a une structure cristalline monoclinique avec le groupe d'espace P21/c (no 14)[6].
Il est soluble dans l'eau et l'éthanol après solvolyse en donnant une solution vert foncé, et sans se décomposer dans des solvants organiques tels que l'éther diéthylique, le chloroforme, le tétrachlorométhane (donnant une solution rouge foncé), ou encore le disulfure de carbone.
Remove ads
Production et réactions
Résumé
Contexte
Le pentachlorure de molybdène peut être obtenu en faisant réagir du molybdène dans du chlore Cl2 en l'absence d'oxygène O2[5]. Avant la réaction, la poudre métallique doit être chauffée à des températures élevées dans un courant d'hydrogène H2 ou d'azote N2 dépourvu d'oxygène pour éliminer tout oxyde de surface. Des précautions doivent alors être prises pour s'assurer que l'air et l'humidité sont complètement éliminés du milieu réactionnel avant la réaction avec le chlore[7] :
On peut également l'obtenir en faisant réagir du trioxyde de molybdène MoO3 avec du tétrachlorométhane CCl4 sous pression[4].
Le pentachlorure de molybdène est réduit par l'acétonitrile CH3CN pour donner un complexe orange MoCl4(CH3CN)2 qui réagit avec le tétrahydrofurane (THF) pour donner le MoCl4(THF)2, précurseur d'autres complexes de molybdène[8].
Le bromure de molybdène(IV) (en) MoBr4 est obtenu par traitement de pentachlorure de molybdène par le bromure d'hydrogène HBr :
Cette réaction fait intervenir du bromure de molybdène(V) MoBr5 instable, qui libère du brome Br2 à température ambiante[9].
Le pentachlorure de molybdène est un bon acide de Lewis envers les ligands non oxydables. Il forme un adduit avec le chlore pour donner [MoCl6]−. En synthèse organique, il peut être utilisé pour réaliser des réactions de chloration, de désoxygénation ou de couplage oxydant[10].
Remove ads
Applications
Le pentachlorure de molybdène peut être utilisé pour déposer du molybdène[11].
Notes et références
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads