Top Qs
Chronologie
Chat
Contexte
Complexe cytochrome b6f
De Wikipédia, l'encyclopédie libre
Remove ads
Le complexe cytochrome b6f, ou complexe de cytochromes b6f, est une oxydoréductase qui catalyse la réaction :
- plastoquinol + 2 plastocyanines oxydées + 2 H+face 1 plastoquinone + 2 plastocyanines réduites + 2 H+face 2.
Cette réaction est analogue à celle catalysée par la coenzyme Q-cytochrome c réductase de la chaîne respiratoire dans les mitochondries. Ce complexe enzymatique est présent dans la membrane des thylakoïdes, organites présents chez les cyanobactéries ainsi qu'à l'intérieur des chloroplastes, eux-mêmes organites photosynthétiques des algues vertes et des plantes. Il a pour fonction d'accumuler des protons dans le lumen des thylakoïdes lors du transfert des électrons à haut potentiel du photosystème II vers le photosystème I.
Remove ads
Structure
Résumé
Contexte
Le complexe cytochrome b6f est un dimère dont chaque monomère est composé de huit sous-unités[2], à savoir quatre grosses sous-unités :
- un cytochrome f avec un cytochrome de type c pour une masse de 32 kDa (sous-unité PetA) ;
- un cytochrome b6 avec un groupe héminique à potentiel haut et potentiel bas pour une masse de 25 kDa (PetB) ;
- une protéine de Rieske contenant un cluster fer-soufre [2Fe-2S] pour une masse de 19 kDa (PetC) ;
- une sous-unité IV de 17 kDa (PetD) ;
et quatre petites sous-unités de 3 à 4 kDa chacune et appelées PetG, PetL, PetM et PetN[2]. La masse totale atteint 217 kDa.
La structure cristallisée de complexes cytochrome b6f de Chlamydomonas reinhardtii, Mastigocladus laminosus and Nostoc sp. PCC 7120 ont été déterminées[1],[3],[4]. La structure du complexe est semblable à celle du cytochrome bc1. Le cytochrome b6 et la sous-unité IV sont semblables au cytochrome b, tandis que les protéines de Rieske des deux complexes sont homologues[5]. Cependant, le cytochrome f et le cytochrome c1 ne sont pas homologues[6].
Le complexe cytochrome b6f contient sept groupes prosthétiques[7],[8]. Quatre d'entre eux sont présents à la fois dans le cytochrome b6f et dans le cytochrome bc1 :
- la molécule d'hème c, présente dans le cytochrome c1 et dans le cytochrome f ;
- les deux molécules d'hème b ;
- le cluster fer-soufre [2Fe-2S] des protéines de Rieske.
Les trois autres groupes prosthétiques ne se trouvent que dans les cytochrome b6f[1] :
- la chlorophylle a ;
- le β-carotène ;
- l'hème cn, également appelé « hème x ».
Remove ads
Fonctionnement biologique
Résumé
Contexte
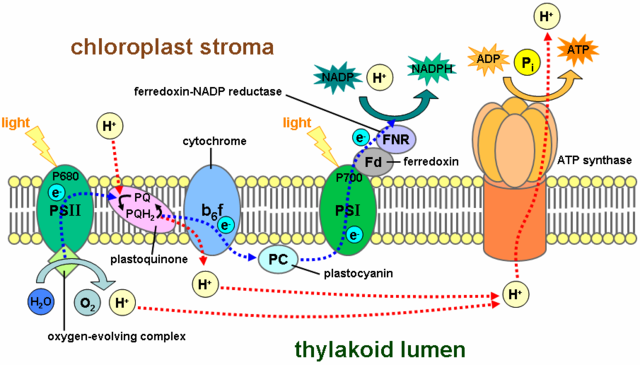
Dans la photosynthèse, le complexe cytochrome b6f intervient dans le transfert des électrons entre deux centres réactionnels, du photosystème II au photosystème I tout en pompant des protons à travers la membrane des thylakoïdes depuis le stroma des chloroplastes vers le lumen des thylakoïdes[9]. C'est la circulation des électrons à travers le complexe cytochrome b6f qui génère le gradient de concentration en protons, et donc le gradient électrochimique, à travers la membrane des thylakoïdes, gradient utilisé pour la phosphorylation de l'ADP en ATP dans les chloroplastes.
À travers une réaction distincte, le complexe cytochrome b6f joue un rôle central dans la photophosphorylation cyclique, lorsqu'il n'y a pas de NADP+ disponible pour recevoir les électrons de la ferrédoxine réduite. Ce cycle intervient également dans le processus de photosynthèse[10] pour maintenir le ratio de production ATP / NADPH approprié pour la fixation du carbone[11].
Remove ads
Notes et références
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads


