Kwaksalwer (ualgreks ὑδράργυρος Hydrargyros ,luupen salwer‘) as en cheemisk element mä det ufkörtang Hg an det atoomnumer 80. Hat as det iansagst luupen metal an böös giftag.
| Eegenskapen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Algemian | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nööm, Symbool, Numer | Kwaksalwer, Hg, 80 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Seerie | Auergungsmetal | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skööl, Periode, Blook | 12, 6, d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klöör, Skak | salwern witj | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-Numer | 7439-97-6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC-Code | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Uundial | 0,4 ppm[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomaar [2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atoommase | 200,592(3)[3] u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atoomraadius (bereegent) | 150 (171) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalent-Raadius | 132 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals-Raadius | 155 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
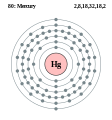
| Elektroonen | [Xe] 4f14 5d10 6s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energii | 4,49 eV[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. Ionisiarang | 1007,1 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. Ionisiarang | 1810 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Füsikaalisk [5] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tustant | luupen | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sachthaid | 13,5459 g/cm3[6] bei 293,15 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hardhaid | entfällt | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetismus | diamagneetisk (Χm = −2,8 · 10−5)[7] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Smoltponkt | 234,32 K (−38,83 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Köögponkt | 630,2 K[8] K (357 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molaar Rüm | (fest) 14,09 · 10−6 m3/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dampwaremk | 58,2 kJ/mol[8] kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Smoltwaremk | 2,37[9] kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dampdruk | 0,163[6] Pa bei 293 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Faard faan a tuun | 1407 m/s bi 293,15 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Waremk | 140 J/(kg · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrisk struumfeerang | 1,04 · 106 A/(V · m) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Waremkfeerang | 8,3 W/(m · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cheemisk [10] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksidatsionstustant | 1, 2, 4[11] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksiiden | Hg2O, HgO | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sür of baasisk | lacht baasisk | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Normoolpotentiaal | 0,8535 V (Hg2+ + 2 e− → Hg) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegatiwiteet | 2,00 (Pauling-Skala) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotoopen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Muar isotoopen bi List faan isotoopen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NMR-Eegenskapen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Seekerhaid | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Muar wäärnangen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| MAK-miat | Sweits: 0,005 ml·m−3 bzw. 0,05 mg·m−3[13] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miast wurd SI-ianhaiden brükt. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Bilen
- Elektroonenskel
- Rian kwaksalwer
- Kwaksalwer uun en gasröör
- En manomeeter mä kwaksalwer
- En baromeeter
- En termomeeter
Luke uk diar
Kwelen
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.