
Química de coordinación
rama da química que estuda ións complexos / From Wikipedia, the free encyclopedia
A química dos compostos de coordinación ou de coordenación é a rama da química que estuda ións complexos, é dicir, moléculas nas que un catión metálico está coordinado ou coordenado (é dicir, unido cun determinado enlace químico) a átomos, ións ou moléculas cun número de enlaces maior que o seu número de oxidación. En particular, esta disciplina trata o estudo do enlace coordinativo, os métodos sintéticos específicos aplicábeis e a caracterización estrutural mediante o uso de técnicas instrumentais como a espectrofotometría infravermella, Mössbauer, fotoelectrónica ou UV / VIS.

En contraste cos enlaces covalentes convencionais, nos complexos os ligandos normalmente achegan todos os electróns ao enlace, en vez de que cada reactivo contribúa cun electrón a un enlace de pares de electróns (enlace coordinativo); non obstante tamén hai complexos de natureza máis covalente[1]. A formación de complexos pode entenderse así como unha reacción ácido-base no sentido da definición de Lewis, na que os ligandos (bases) actúan como doadores de pares de electróns e a partícula central (ácido) como aceptor a través de ocos na súa configuración electrónica.
Existen varios tipos de complexos que van desde o simple metal en solución acuosa coordinado por moléculas de auga até os complexos metal-encima ou proteína metálica, teñen múltiples funcións e aplicacións e hoxe abarcan gran parte da investigación en química inorgánica.
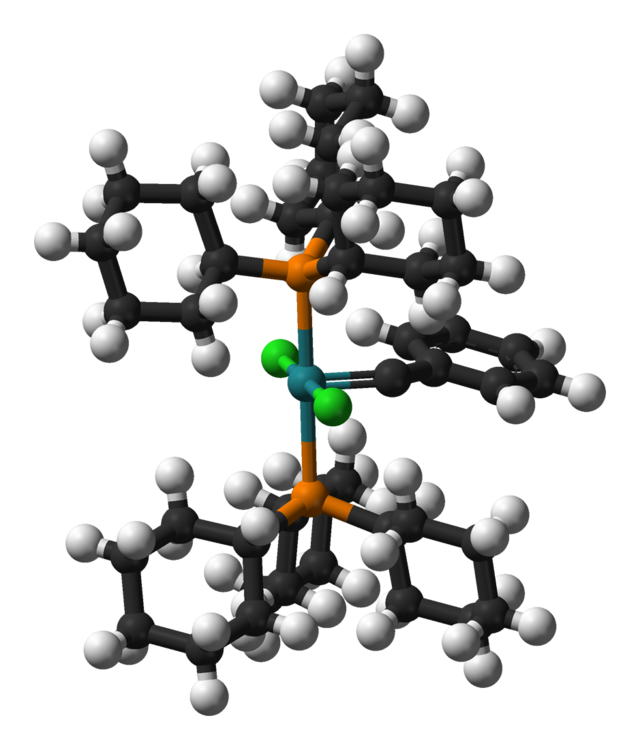
Unha grande importancia na investigación e na química dos complexos en xeral é que poden ser catalizadores de fase homoxéneos para as reaccións químicas (ver figura do catalizador Grubbs á dereita).
Os complexos, que implican os orbitais do metal no enlace, son moi frecuentemente coloreados, por exemplo, o Fe coordinado coa hemoglobina o que lle dá ao sangue a cor vermella. No corpo humano o Fe (II) está presente en hemoglobina e mioglobina, coordinados cos átomos de nitróxeno do anel de porfirina (grupo hemo da proteína) e realiza a función de unir o osíxeno que logo será transportado a través do sangue até os tecidos. Moitos encimas tamén necesitan formar complexos con metais para desempeñar a súa función.
Dado que os complexos de metais de transición son ás veces moi coloridos, tamén se utilizan como tinturas ou pigmentos (azul de Berlín ou azul de Prusia). Esta característica pódese aproveitar na valoración ou análise volumétrica.
Durante moito tempo, os químicos non tiñan idea da estrutura dos compostos coordinativos chamados "compostos de orde superior". Ademais, moitos comportamentos dos complexos non poderían ser explicados polas teorías da época, como a estabilidade do cloruro de cobalto (III) en solución acuosa coa adición de amoníaco. Para a correcta interpretación das relacións estruturais e de unión en complexos, o suízo Alfred Werner foi o primeiro e durante décadas único inorgánico en recibir o Premio Nobel de Química en 1913.