
Bikarbonat
senyawa kimia / From Wikipedia, the free encyclopedia
Untuk baking soda, lihat natrium bikarbonat. Untuk prinsip pemrograman, lihat Tim Toady Bicarbonate.
"Hidrogen karbonat" beralih ke halaman ini. Untuk asam okso, lihat asam karbonat.
Dalam kimia anorganik, bikarbonat (tatanama yang direkomendasikan oleh IUPAC: hidrogen karbonat[2]) adalah bentuk antara dari deprotonasi asam karbonat. Ia merupakan anion poliatomik dengan rumus kimia HCO−3.
Fakta Singkat Nama, Penanda ...
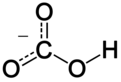 | |
 | |
| Nama | |
|---|---|
| Nama IUPAC (sistematis)
Hydroxidodioxidocarbonate(1−)[1] | |
| Nama lain
Hydrogencarbonate[1] | |
| Penanda | |
| |
Model 3D (JSmol) |
|
| 3DMet | {{{3DMet}}} |
| Referensi Beilstein | 3903504 |
| ChEBI | |
| ChEMBL | |
| ChemSpider |
|
| Nomor EC | |
| Referensi Gmelin | 49249 |
| KEGG |
|
PubChem CID |
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA) |
|
| |
| |
| Sifat | |
| HCO−3 | |
| Massa molar | 61,0168 g mol−1 |
| log P | −0,82 |
| Keasaman (pKa) | 10,3 (Asam konjugat dari karbonat) |
| Kebasaan (pKb) | 7,7 (Basa konjugat dari asam karbonat) |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Tutup
Bikarbonat mempunyai peran biokimia penting dalam sistem pendaparan pH fisiologis.[3]
Istilah "bikarbonat" diberikan pada tahun 1814 oleh kimiawan Inggris William Hyde Wollaston.[4] Awalan "bi" dalam "bikarbonat berasal dari sistem penamaan kuno dan berdasarkan pengamatan bahwa terdapat dua karbonat (CO2−3) per ion natrium dalam natrium bikarbonat (NaHCO3) dan bikarbonat lain kecuali dalam natrium karbonat (Na2CO3) dan karbonat lainnya.[5] Nama tersebut masih lestari sebagai nama trivial.