
Geometri molekul oktahedral
From Wikipedia, the free encyclopedia
Dalam kimia, geometri molekul oktahedral menggambarkan bentuk senyawa dengan enam atom atau kelompok atom atau ligan yang tersusun secara simetris di sekitar atom pusat, yang menentukan simpul simpul oktahedron. Oktahedron memiliki delapan muka, maka diberi awalan okta yang berarti delapan. Oktahedron adalah salah satu padatan Platonis, walaupun molekul oktahedral biasanya memiliki atom di pusatnya dan tidak ada ikatan antara atom-atom ligan. Suatu oktahedron sempurna termasuk dalam kelompok titik Oh. Contoh senyawa oktahedral adalah belerang heksafluorida SF6 dan molibdenum heksakarbonil Mo(CO)6. Istilah "oktahedral" digunakan agak longgar oleh kimiawan, dengan fokus pada geometri ikatan ke atom pusat dan tidak mempertimbangkan perbedaan di antara ligan sendiri. Misalnya, [Co(NH' Too many ('";, yang tidak oktahedral dalam pengertian matematis karena orientasi ikatan N-H, tetap disebut sebagai oktahedral.[1]
| Geometri molekul oktahedral | |
|---|---|
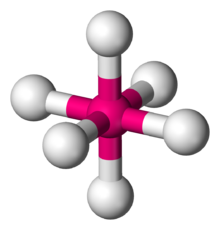 | |
| Contoh | SF6, Mo(CO)6 |
| Kelompok titik | Oh |
| Bilangan sterik | 6 |
| Bilangan koordinasi | 6 |
| Sudut ikatan | 90° |
| μ (Polaritas) | 0 |

Konsep geometri koordinasi oktahedral dikembangkan oleh Alfred Werner untuk menjelaskan stoikiometri dan isomerisme pada senyawa koordinasi. Pandangannya memungkinkan kimiawan untuk merasionalisasi jumlah isomer dalam senyawa koordinasi. Kompleks logam transisi oktahedral yang mengandung amina dan anion sederhana sering disebut sebagai kompleks tipe Werner.