Timeline
Chat
Prospettiva
Nitrosilazoturo
composto chimico Da Wikipedia, l'enciclopedia libera
Remove ads
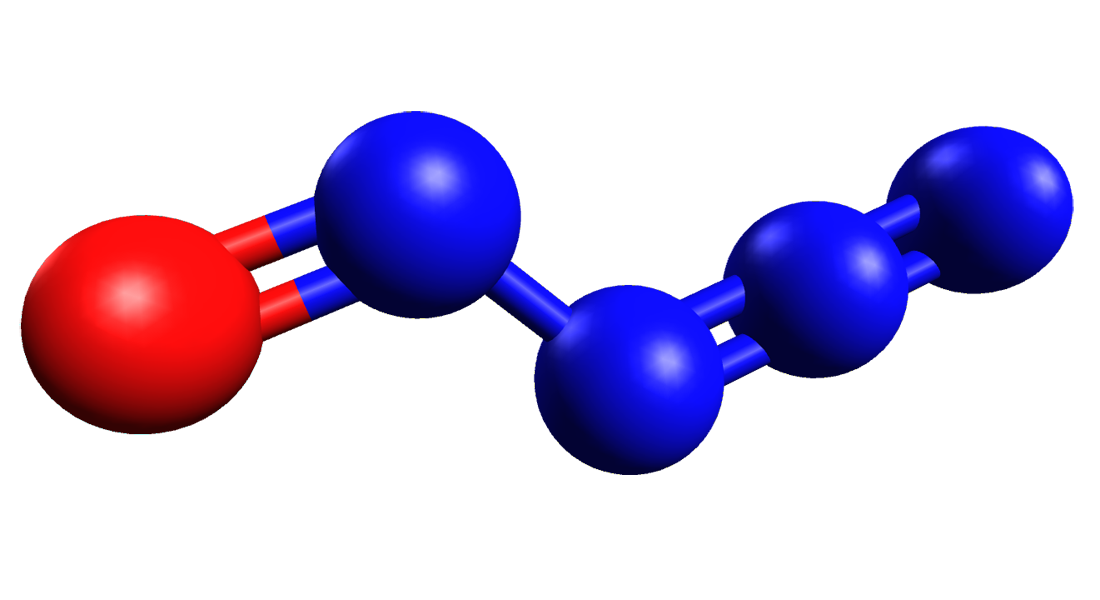
Il nitrosilazoturo è un ossido di azoto altamente instabile, con formula chimica N4O. È un composto inorganico a legame covalente delle pozioni-molecole di azoturo e di nitrosile. Il contenuto di azoto nella molecola è del 77,79 %.
Remove ads
Sintesi
La prima sintesi fu effettuata nel 1958 dal chimico H. W. Lucien. Tale sintesi avviene tramite la seguente reazione di azoturo di sodio e cloruro di nitrosile a bassa temperatura:[4][5]
Sotto −50 °C, il composto esiste come un solido giallo pallido, nella forma d'isomero geometrico tipo trans. Il prodotto è ottenuto per distillazione sotto vuoto dalla miscela di reazione.
Sopra questa temperatura, si decompone in monossido di diazoto (N2O) e azoto molecolare (N2):
Invece del cloruro di nitrosile si possono usare come fonti di NO, l'acido nitrosilsolforico oppure l'acido nitroso.[5]
Remove ads
Proprietà
Riepilogo
Prospettiva
La pressione di vapore in funzione della T è data dall'equazione di Antoine come lg(P) = −A/T+B (P in Torr, T in Kelvin) con A = 1215,6 e B = 7,306.[5] Per estrapolazione, è possibile stimare un normale punto di ebollizione della pressione alla temperatura T=1,5 °C. Questo punto non può essere raggiunto praticamente perché abbiamo detto che il composto si decompone sopra a -50 °C. Un calcolo ab initio di chimica quantistica ha rivelato un calore fortemente esotermico di reazione con -381 kJ · mol-1 a -50 °C.
La caratterizzazione è stata effettuata mediante spettroscopia infrarossa[5] e Raman[4], per cui le bande misurate si accordano bene con i valori teorici calcolati per un isomero geometrico trans. I calcoli chimico-quantistici hanno rivelato un isomero di tipo cis a energia di 4,2 kJ · mol-1 e un isomero di struttura aromatico di anello 6π più stabile intorno a 54,4 kJ · mol-1. Per la reazione di ciclizzazione, si dovrebbe applicare un'energia di attivazione molto elevata di 205 kJ · mol-1 a causa della flessione della funzione dell'azoturo. [4]
Questo può essere visto come una ragione per cui il nitrosilazoturo è così stabile e può essere isolato a basse temperature. La forma ciclica si decompone rapidamente come visto precedentemente.
Remove ads
Note
Bibliografia
Altri progetti
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads