
gp120 (HIV)
ウィキペディア フリーな encyclopedia
gp120(envelope glycoprotein gp120)は、HIVのエンベロープ表面に露出している糖タンパク質である。このタンパク質は、ハーバード公衆衛生大学院のTun-Hou Lee(李敦厚)、Max Essexらによって1984年に発見された[1]。120という数字はその分子量が約120kであることに由来している。gp120はウイルスが細胞へ侵入する際に必要不可欠であり、細胞表面受容体への特異的な接着に重要な役割を果たしている。こうした受容体としてはDC-SIGN(英語版)[2]やヘパラン硫酸プロテオグリカン[3]が知られており、特にヘルパーT細胞上ではCD4と特異的相互作用を行う[4]。CD4への結合によって、gp120やgp41(英語版)のコンフォメーション変化カスケードの開始が誘導され、ウイルス膜と宿主の細胞膜との融合が引き起こされる。CD4への結合にはファンデルワールス相互作用や水素結合も関与しているものの、主に静電的相互作用によって媒介されている[5]。
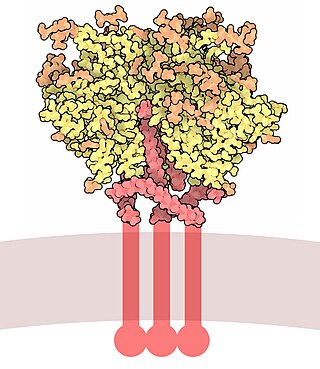
| Envelope glycoprotein gp120 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 識別子 | |||||||||
| 略号 | GP120 | ||||||||
| Pfam | PF00516 | ||||||||
| InterPro | IPR000777 | ||||||||
| SCOP | 1gc1 | ||||||||
| SUPERFAMILY | 1gc1 | ||||||||
| |||||||||
| テンプレートを表示 | |||||||||
gp120はHIVのenv(英語版)遺伝子にコードされている。この遺伝子の長さは約2.5 kbで、約850アミノ酸のタンパク質がコードされている[6]。env遺伝子に由来するタンパク質の一次産物はgp160であり、小胞体内で宿主のプロテアーゼであるフーリンによってgp120(約480アミノ酸)とgp41(約345アミノ酸)へと切断される[7]。gp120のコア領域の結晶構造から、inner domain、outer domain、bridging sheetと呼ばれる3つの領域からなる構成をしていることが示されている。gp120は膜貫通型糖タンパク質gp41との非共有結合的結合を介してウイルスの膜(エンベロープ)に固定されている。宿主細胞への接着と侵入を媒介するエンベロープのスパイクタンパク質はgp120とgp41それぞれ3分子ずつから構成され、gp120-gp41ヘテロ二量体が三量体化するかたちで形成されている[8]。