トップQs
タイムライン
チャット
視点
シトクロムcオキシダーゼ
ウィキペディアから
Remove ads
シトクロムcオキシダーゼ (cytochrome c oxidase, COX) または複合体IV(Complex IV)またはcytochrome a3 は、バクテリアおよびミトコンドリアで見られる膜貫通タンパク質複合体の一つである。
ミトコンドリア膜(またはバクテリア膜)における電子伝達系の最後の酵素であり、4分子のシトクロムcからそれぞれ電子を受け取り、酸素1分子に転移させ2分子の水に変換する機能を持つ。この過程では、マトリックス由来の4個のプロトンから水が生成されるのと同時に4個のプロトンがマトリックスから膜間スペースに透過する。これにより発生した膜間の電気化学ポテンシャルの差がATP合成酵素によるATP合成に用いられる。
Remove ads
構造
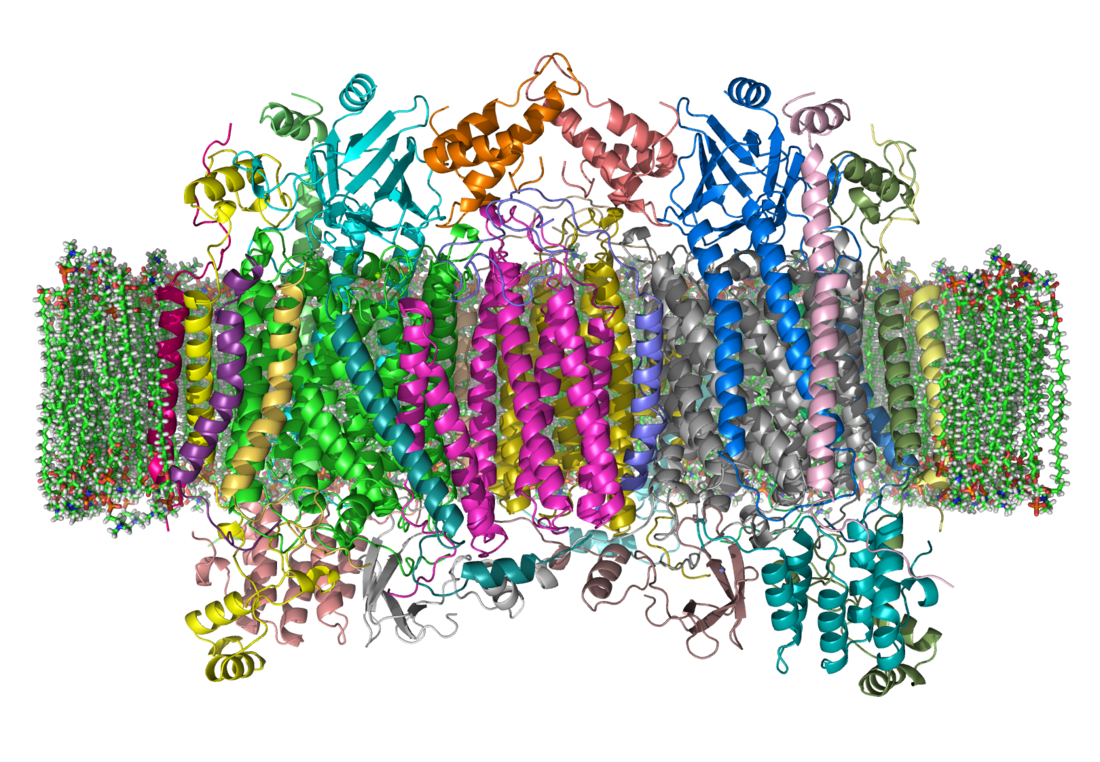
複合体IVは、哺乳類では、いくつかの金属補欠分子族部位と13のタンパク質サブユニットから構成される巨大な内在性膜タンパク質である。哺乳類では、10個のサブユニットは核由来で、残りの3個はミトコンドリアで合成される。複合体IVには2種のヘム(ヘムa 、ヘムa 3)、2種の銅中心(CuAとCuB)が含まれている[1]。2種類のヘム(ヘムa、ヘムa 3)とCuBはサブユニットIに位置し、2個のCuAはサブユニットIIに配位している。サブユニットIのヘムa 3とCuBはそれぞれで二核中心を形成し、酸素の還元部位となっている。
シトクロムc は、複合体IIIのシトクロムc 1によって還元された後、複合体IVのCuA二核中心と結合し、シトクロムc の鉄中心はFe2+からFe3+に酸化される。還元されたCuA二核中心はその電子をヘムa に送り、さらにそこからヘムa 3-CuB二核中心に送られる。この二核中心の2個の金属イオンは4.5 Å離れており、十分な酸化状態の水酸化物イオンに配位している。
シトクロムc の結晶学的研究では、Tyr(244)のC6とHis(240)のε-Nが結合するという独特な翻訳後修飾が見られた(ウシ亜科のクロムcオキシダーゼでの酵素ナンバーリング)。これにより、ヘムa 3-CuB二核中心が4電子を受け取って酸素分子を水に還元するという極めて重要な役割が可能になっている。以前は、還元機構は過酸化物中間体が関与していると考えられ、それが超酸化物の生成に繋がっていると考えられていた。しかし、現代では、4電子還元によって酸素-酸素結合が開裂する反応機構が支持されており、超酸化物が形成しそうな中間体は避けられている[2]。
Remove ads
生化学
要約
視点
反応の概要:
- フェロシトクロムフェリシトクロム
ここで、
- フェロシトクロム = シトクロム
- フェリシトクロム = シトクロム
まず、2個の電子がシトクロムcから、CuA二核中心とヘムa を通過して、ヘムa 3-CuB二核中心に至り、このFe3+はFe2+に、Cu2+はCu+に還元される。このときそれぞれの金属イオンに配位していたヒドロキシル配位子はプロトン化されて水として失われ、金属間に酸素分子が入る空間が作られる。酸素はFe2+-シトクロム c由来の2電子により迅速に還元され、フェリオキソ型(Fe+4=O)に変換される。CuB側の酸素原子はCu+からの1電子と、Tyr(244)の由来の1電子と1プロトンを受け取りヒドロキシ配位子に変換される。このときTyr(244)はチロシルラジカルとなる。別のシトクロムc から発生する3番目の電子は始めの2種の電子キャリアーからヘムa 3-CuBに至り、この電子と2プロトンによりチロシルラジカルがチロシンに戻り、そしてヒドロキシドはCuB2+に結合し後に水分子となる。同様に4番目の電子も始めの2種の電子キャリアーからヘムa 3-CuBに至ることによりFe+4=OがFe+3に還元され、同時に酸素原子がプロトンを受け取り、ヘムa 3-CuBがこのサイクルの始めの状態に戻る。まとめると、4分子の還元型シトクロムc と4個のプロトンが用いられ酸素分子を2分子の水に還元していることになる。
Remove ads
抑制
シアニド、スルフィド、アジドおよび一酸化炭素[3]の全てがシトクロムcオキシダーゼに結合し、拮抗的阻害を及ぼし細胞を化学的な窒息状態にさせる。また、メタノール(メチル化剤)はホルムアルデヒドに変換され、こちらも同じように系を阻害する。
資料画像
- シトクロムcオキシダーゼの構造
- シトクロムcオキシダーゼの反応機構の模式図
- シトクロムcオキシダーゼの酸化還元サイクル
- 電子伝達系
脚注
関連項目
外部リンク
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads


![{\displaystyle {\mathrm {c} \ {}+{}8\,\mathrm {H} {\vphantom {A}}^{+}{\vphantom {A}}_{\smash[{t}]{\mathrm {in} }}\ {}+{}\mathrm {O} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}4}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/6751c7442856de55372ff9b96bc0fda19bd3f663)
![{\displaystyle {\mathrm {c} \ {}+{}2\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} \ {}+{}4\,\mathrm {H} {\vphantom {A}}^{+}{\vphantom {A}}_{\smash[{t}]{\mathrm {out} }}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/3488c76d27d44a9ef06a4c3f9cd51d1e6c0e1228)






