
ゲフィチニブ
抗がん剤の一つ / ウィキペディア フリーな encyclopedia
親愛なるWikiwand AI, これらの重要な質問に答えるだけで、簡潔にしましょう:
トップの事実と統計を挙げていただけますか ゲフィチニブ?
この記事を 10 歳向けに要約してください
すべての質問を表示
ゲフィチニブ(Gefitinib)は、上皮成長因子受容体 (EGFR) のチロシンキナーゼを選択的に阻害する内服抗がん剤。癌の増殖などに関係する特定の分子を狙い撃ちする分子標的治療薬の一種である。 商品名はイレッサ (Iressa) で、アストラゼネカが製造・販売[1]。褐色の錠剤で一錠250mgのゲフィチニブを含有する。ゲフィチニブ製剤は手術不能または再発した非小細胞肺癌に対する治療薬として用いられる。
概要 IUPAC命名法による物質名, 臨床データ ...
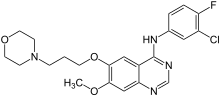 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 胎児危険度分類 |
|
| 法的規制 | |
| 投与経路 | 経口投与 |
| 薬物動態データ | |
| 生物学的利用能 | 59%(経口時) |
| 血漿タンパク結合 | 90% |
| 代謝 | 肝臓(主にCYP3A4) |
| 半減期 | 6時間 - 49時間 |
| 排泄 | 糞中86%、尿中4%未満 |
| 識別 | |
| CAS番号 | 184475-35-2 |
| ATCコード | L01XX31 (WHO) |
| PubChem | CID: 123631 |
| KEGG | D01977 |
| 化学的データ | |
| 化学式 | C22H24ClFN4O3 |
| 分子量 | 446.902 |
| テンプレートを表示 | |
閉じる
イレッサは2002年7月5日、世界に先駆けて日本で承認され、2003年5月5日、アメリカ食品医薬品局 (FDA) での承認[2]を含め、いくつかの国で承認を受けた。しかし、無作為比較臨床試験(ISEL試験[3]、後述)の結果、プラセボと比較して生存期間を延長することができなかったため、2005年1月4日アストラゼネカは欧州医薬品局 (EMEA) への承認申請を取り下げ[4]、また2005年6月17日、FDAは本薬剤の新規使用を原則禁止とした[5]。その後2009年7月1日、欧州医薬品局は、後述のINTEREST試験とIPASS試験の2つの無作為化第III相臨床試験の結果をもとに、成人のEGFR遺伝子変異陽性の局所進行または転移を有する非小細胞肺癌を対象にイレッサの販売承認を行った[6]。2009年現在イレッサを承認している国は、日本を含めたアジア諸国、欧州、オーストラリア、メキシコ、アルゼンチンである。ゲフィチニブは白色から黄白色の粉末。開発コード名ZD1839。