글루탐산
화합물 / From Wikipedia, the free encyclopedia
글루탐산(영어: glutamic acid) (기호: Glu or E)[4]은 단백질의 생합성에 사용되는 α-아미노산이다. 이온형은 글루탐산염(영어: glutamate)으로 알려져 있다. 글루탐산은 사람에게 필수적이지 않으며, 인체에서 합성될 수 있다. 글루탐산은 또한 흥분성 신경전달물질로 척추동물의 신경계에 풍부하다. 글루탐산은 GABA작동성 뉴런에서 억제성 γ-아미노뷰티르산(GABA)의 합성을 위한 전구체 역할을 한다.
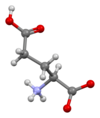
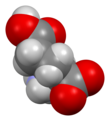
 L-글루탐산의 골격 구조식 | |||
| |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름
glutamic acid | |||
| 체계명
2-aminopentanedioic acid | |||
| 별칭
2-aminoglutaric acid | |||
| 식별자 | |||
3D 모델 (JSmol) |
| ||
| 3DMet |
| ||
| 1723801 (L) 1723799 (rac) 1723800 (D) | |||
| ChEBI |
| ||
| ChEMBL |
| ||
| ChemSpider |
| ||
| DrugBank | |||
| ECHA InfoCard | 100.009.567 | ||
| EC 번호 |
| ||
| E 번호 | E620 (조미료) | ||
| 3502 (L) 101971 (rac) 201189 (D) | |||
| KEGG | |||
PubChem CID |
|||
| UNII |
| ||
CompTox Dashboard (EPA) |
| ||
| |||
| |||
| 성질 | |||
| C5H9NO4 | |||
| 몰 질량 | 147.130 g·mol−1 | ||
| 겉보기 | 흰색 결정성 분말 | ||
| 밀도 | 1.4601 (20 °C) | ||
| 녹는점 | 199 °C (390 °F; 472 K) 분해 | ||
| 7.5 g/L (20 °C)[1] | |||
| 용해도 | 에탄올: 350 μg/100 g (25 °C)[2] | ||
| 산성도 (pKa) | 2.10, 4.07, 9.47[3] | ||
자화율 (χ) |
−78.5·10−6 cm3/mol | ||
| 위험 | |||
| GHS 그림문자 |  | ||
| 신호어 | 경고 | ||
GHS 유해위험문구 |
H315, H319, H335 | ||
GHS 예방조치문구 |
P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405, P501 | ||
| NFPA 704 (파이어 다이아몬드) | |||
글루탐산의 분자식은 C
5H
9NO
4이다. 글루탐산은 세 가지 광학 이성질체 형태로 존재한다. L-글루탐산은 일반적으로 글루텐의 가수분해 또는 사탕무 제조 과정의 폐수 또는 발효에 의해 얻을 수 있다.[5] 글루탐산의 분자 구조는 HOOC−CH(NH
2)−(CH
2)2−COOH로 나타낼 수 있으며, 2개의 카복실기(−COOH)와 1개의 아미노기(−NH
2)를 가지고 있다. 그러나 고체 상태 및 약산성 수용액에서 분자는 전기적으로 중성인 −OOC−CH(NH+
3)−(CH
2)2−COOH의 양쪽성 이온 구조로 간주된다. 글루탐산은 GAA, GAG 코돈에 의해 암호화되어 있다.
글루탐산은 두 번째 카복실기에서 1개의 양성자를 잃어 짝염기인 단일 음성 음이온 글루탐산염인 −OOC−CH(NH+
3)−(CH
2)2−COO−를 형성할 수 있다. 이러한 형태는 중성 용액에서 널리 발견할 수 있다. 신경전달물질로서 글루탐산은 신경의 활성화에 중요한 역할을 한다.[6] 글루탐산 음이온은 음식에서 감칠맛을 내며, 글루탐산 일나트륨(MSG)과 같은 글루탐산 향미료에서 발견된다. 유럽에서 글루탐산은 식품 첨가물 E620으로 분류된다. 고알칼리성 용액에서는 이중 음이온 형태인 −OOC−CH(NH
2)−(CH
2)2−COO−가 우세하다. 글루탐산에 해당하는 라디칼을 글루타밀(영어: glutamyl)이라고 한다.