Loading AI tools
화합물 위키백과, 무료 백과사전
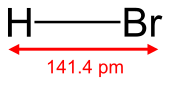
브로민화 수소(영어: hydrogen bromide, HBr)는 상온 상태에서는 무색의 기체이다. 물에 용해하면 브로민화 수소산을 얻게 되고, 반대로 탈수제(脫水劑)의 첨가를 통해 기체를 추출해낼 수도 있지만, 수소산이 용해된 물을 단순히 증류시키는 방법으로는 같은 효과를 기대할 수 없다.
 | |||
| |||
| 이름 | |||
|---|---|---|---|
| 우선명 (PIN)
Hydrogen bromide | |||
| 체계명
Bromane[1] | |||
| 식별자 | |||
3D 모델 (JSmol) |
|||
| 3587158 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.030.090 | ||
| EC 번호 |
| ||
| KEGG | |||
| MeSH | Hydrobromic+Acid | ||
PubChem CID |
|||
| RTECS 번호 |
| ||
| UNII | |||
| UN 번호 | 1048 | ||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| 성질 | |||
| HBr | |||
| 몰 질량 | 80.91 g/mol | ||
| 겉보기 | Colorless gas | ||
| 냄새 | Acrid | ||
| 밀도 | 3.6452 kg/m3 (0 °C, 1013 mbar)[2] | ||
| 녹는점 | −86.9 °C (−124.4 °F; 186.2 K) | ||
| 끓는점 | −66.8 °C (−88.2 °F; 206.3 K) | ||
| 221 g/100 mL (0 °C) 204 g/100 mL (15 °C) 193 g/100 mL (20 °C) 130 g/100 mL (100 °C) | |||
| 용해도 | Soluble in alcohol, organic solvents | ||
| 증기 압력 | 2.308 MPa (at 21 °C) | ||
| 산성도 (pKa) | −8.8 (±0.8);[3] ~−9[4] | ||
| 염기도 (pKb) | ~23 | ||
| 짝산 | Bromonium | ||
| 짝염기 | Bromide | ||
굴절률 (nD) |
1.325 | ||
| 구조 | |||
| Linear | |||
| 820 mD | |||
| 열화학 | |||
열용량 (C) |
350.7 mJ/(K·g) | ||
표준 몰 엔트로피 (S |
198.696–198.704 J/(K·mol)[5] | ||
표준 생성 엔탈피 (ΔfH⦵298) |
−36.45...−36.13 kJ/mol[5] | ||
| 위험 | |||
| 물질 안전 보건 자료 | hazard.com | ||
| GHS 그림문자 |   | ||
| 신호어 | 위험 | ||
GHS 유해위험문구 |
H314, H335 | ||
GHS 예방조치문구 |
P261, P280, P305+351+338, P310 | ||
| NFPA 704 (파이어 다이아몬드) | |||
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |||
LC50 (median concentration) |
2858 ppm (rat, 1 h) 814 ppm (mouse, 1 h)[6] | ||
| NIOSH (미국 건강 노출 한계): | |||
PEL (허용) |
TWA 3 ppm (10 mg/m3)[7] | ||
REL (권장) |
TWA 3 ppm (10 mg/m3)[7] | ||
IDLH (직접적 위험) |
30 ppm[7] | ||
| 관련 화합물 | |||
관련 화합물 |
Hydrogen fluoride Hydrogen chloride Hydrogen iodide Hydrogen astatide | ||
브로민화 수소는 상온 상태에서는 신랄한 냄새가 나는 비휘발성 기체로, 습도 높은 공기와 접촉하면 수소산을 형성하기 시작한다. 물에 잘 녹으며, 298K에서 물에 용해하면 물 중량의 68.85%가 수소산화한 후 포화 상태가 된다. 전체 무게의 47.38%가 용해된 브롬화 수소로 구성된 물은 126 °C에서 끓는 공비 혼합물(azeotropte)이 되는데, 용해된 브로민화 수소의 비율이 더 낮을 경우 H2O는 브로민화 수소의 함유량이 47.38%에 이를 때까지 100 °C에서 계속 증발한다.
브로민화 수소로 알코올에서 브로민화 알킬(alkyl bromide)을 추출한다.
알켄에서 분리한 브로민을 첨가해 중요한 유기브로민 화합물(organobromine compound)의 하나인 브로모알케인(bromoalkane)을 이룬다.
알카인에 첨가하여 브로모알켄(bromoalkene)을 생산한다. 입체화학에서는 이런 류의 첨가 반응을 안티(anti)라고 한다.
할로알켄(haloalkene)에 첨가하여 두 브로민 원자가 탄소 원자와 연결된 이중 할로알케인(dihaloalkane)을 만든다. 이런 첨가 반응은 마르코프니코프의 법칙(Markovnikov's rule)을 따른다.
브로민화 수소는 에폭시 화합물(epoxide)이나 락톤(lactone)을 열거나 브로모아세탈(bromoacetal)을 합성하는 데에도 쓰이고, 촉매 용도로도 사용된다.[8][9][10][11]
브로민화 수소(브로민화 수소산 포함)는 비슷한 특성을 가진 염화물(chloride)보다 훨씬 더 적은 양이 산출된다. 공업용으로는 수소와 브로민을 200-400 °C에서 대개 백금이나 석면(石綿)을 촉진제로 활용해 제조한다.[9][12]
브로민화 수소는 여러 방법으로 합성할 수 있다. 편리한 방법의 하나는 브로민화 나트륨(NaBr)과 강산(強酸)을 이용하는 것인데[13], 생성된 브로민화 수소를 다시 산화해버리는 황산은 예외이다.
브로민화 수소를 산화하지 않는 인산(燐酸) 등은 써도 무방하다.
테트랄린(tetralin - 1,2,3,4-tetrahydronaphthalene)을 사용하면 이렇게 된다.[13]
무수(無水)의 브로민화 수소는 환류하는 자일렌(xylene) 내 트라이페닐포스포늄(triphenylphosphonium)의 열분해(thermal decomposition)를 통해서도 소량을 생산할 수 있다.[8]
위에서 열거한 방법들의 경우 결과물이 브로민 가스(Br2)로 오염되어 있을 수 있는데, 결과가 나온 후 구리로 된 선반이나 페놀 사이로 통과시키면 문제를 해결할 수 있다.[12]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.