Top Qs
Linha do tempo
Chat
Contexto
Decaborano
composto químico Da Wikipédia, a enciclopédia livre
Remove ads
Decaborano, também chamado decaborano(14), é o borano de fórmula química B10H14. Este composto cristalino branco é um dos principais clusteres de hidreto de boro, como estrutura de referência e como precorsor para outros hidretos de boro.
Este artigo não cita fontes confiáveis. (Junho de 2021) |
Remove ads
Manuseio e propriedades
O decaborano 14 possui um forte odor característico, algumas vezes descrito como semelhante ao mofo, à borracha ou intensamente amargo, parecido com chocolate que é exclusivo para boranos. As características físicas do decaborano-14 se assemelham às dos compostos orgânicos, tais como naftaleno e antraceno, na medida em que pode ser sublimado sob vácuo a temperaturas moderadas. A sublimação é o método comum de purificação. Como os compostos orgânicos, decaborano é altamente inflamável, mas, como outros hidretos de boro, ele queima com uma chama verde brilhante. Não é sensível ao ar úmido, embora sofra hidrólise em água fervente, liberando hidrogênio e dando uma solução de ácido bórico. É solúvel em água fria, bem como uma variedade de solventes não-polares e moderadamente polares.[1]
Remove ads
Estrutura



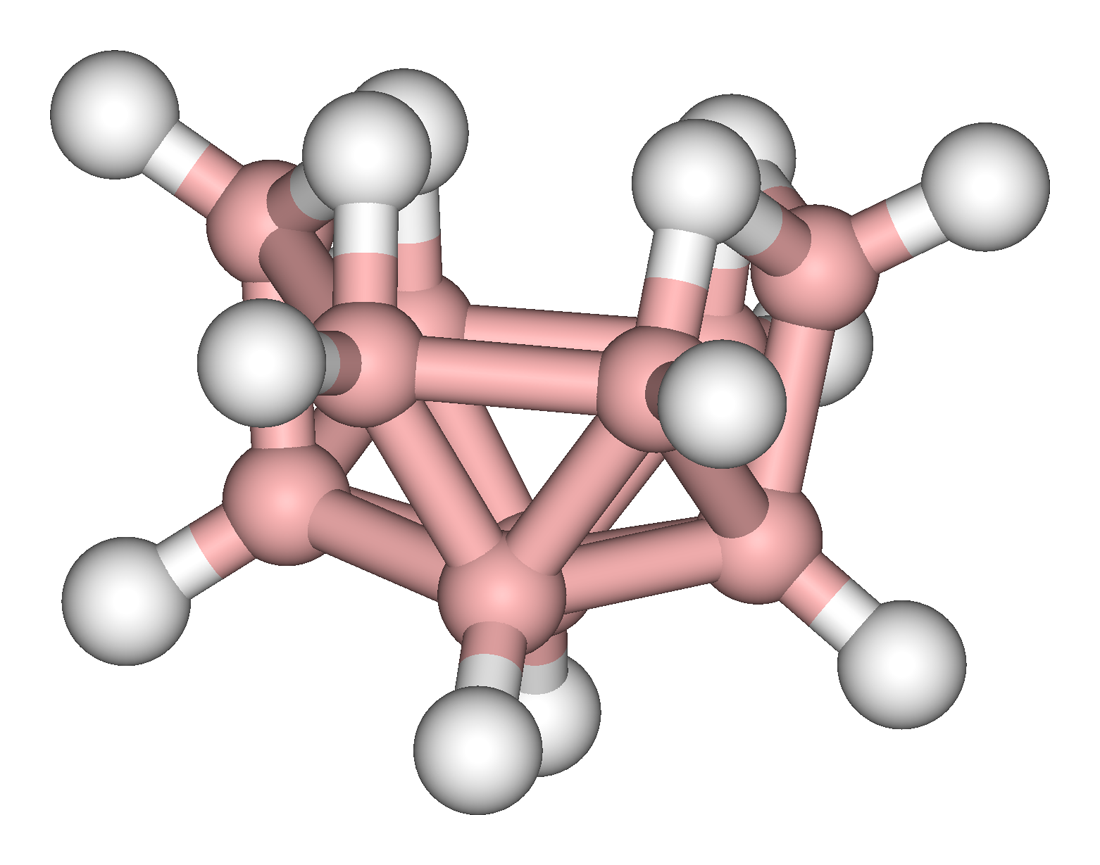
O esqueleto da estrutura do decaborano se assemelha a um octadecaedro incompleto, ou a um icosaedro com dois vértices vizinhos faltantes. Cada vértice da gaiola é composto por um grupo B–H radial, e quatro átomos de boro, próximos à parte aberta do cluster, possuem hidrogênios extra ligados. As ligações entre os boros e os hidrogênios ligados radialmente são ligações covalentes simples normais (embora o hidrogênio fique com uma carga parcial negativa, por ser mais eletronegativo do que o boro), enquanto as ligações entre os átomos de boro dentro da gaiola são consideradas como um híbrido de ressonância entre ligações covalentes normais e ligações do tipo ligação covalente tricentrada com dois elétrons (3c-2e).[2] Há um total de duas ligações covalentes normais B–B, seis ligações tricentradas B---B---B, quatro ligações tricentradas B---H---B e dez ligações normais B–H. Os quatro hidrogênios extra da parte aberta da gaiola são ligados aos boros por ligações 3c-2e. Na linguagem da química cluster, a estrutura é classificada como "nido".[3]
Remove ads
Sínteses e reações
é comumente sintetizado através da pirólise de clusters menores de hidreto de boro. Por exemplo, o aquecimento do diborano ou do pentaborano B5H9 dá decaborano, com perda de H2[4]. Em escala laboratorial, o borohidreto de sódio é tratado com trifluoreto de boro para produzir NaB
11H
14
, que é acidificado para liberar decaborano e gás hidrogênio.[5]
O decaborano reage com bases de Lewis (L), tais como CH3CN e (CH3)2S, para formar derivados com a fórmula B10H12·2L.[6][7]
- B10H14· + 2L → B10H12L2· H2
Essas espécies, que são classificados como clusters do tipo "aracno", por sua vez, reagem com o acetileno para dar um "closo" orto-carborano:[8]
- B10H12L2 + C2H2 → C2B10H12 + 2L + H2
Ele é um ácido de Brønsted fraco. A eliminação de um próton gera o ânion [B10H13]-, com uma nova estrutura do tipo nido.
Aplicações
Resumir
Perspectiva
O decaborano não tem aplicações importantes, embora tenha sido frequentemente investigadas. Uma vez que a molécula se decompõe em um plasma, produzindo íons de boro monoatómico, o decaborano é potencialmente útil como um combustível para fusão aneutrônica, e para a implantação de íons de boro de baixa energia na fabricação de semicondutores.[9] Também foi considerado para a deposição assistida de plasma de vapor químico para a fabricação de filmes finos contendo boro. No estudo sobre a fusão, a habilidade do boro de absorver nêutrons tem levado ao uso desses filmes finos de boro para "boronizar" as paredes da câmara de vácuo do tokamak para reduzir a reciclagem de partículas e impurezas no plasma e melhorar o desempenho global.[10]
O decaborano é um reagente eficaz para a aminação redutiva de cetonas e aldeídos.[11]
Decaborano também foi estudado como um aditivo para combustíveis especiais de alto desempenho de foguetes.[12][13] Seus derivados foram investigados, como por exemplo o dietil-decaborano. Um combustível de composição patenteada inclui o copolímero de decaborano com poliéster vinílico. Vinil-decaborano ("dekene") é preparado reagindo-se o decaborano com o acetileno[14].
Remove ads
Segurança
O decaborano, assim como o pentaborano, é uma toxina poderosa que afeta o sistema nervoso central, embora o decaborano seja menos tóxico que o pentaborano. Ele pode ser absorvido pela pele.
A purificação por sublimação requer um vácuo dinâmico para remover os gases desenvolvidos. Amostras brutas explodem perto de 100°C.
Ele pode formar uma mistura explosiva com o tetracloreto de carbono, o que causou uma explosão, muitas vezes citada em uma fábrica de Malta, NY em 1948, quando CCl4 foi usado para limpar o equipamento.[15]
Na forma cristalina, reage violentamente com ácido nítrico fumegante vermelho e branco, que tem uso como oxidante de combustível de foguete, produzindo uma detonação extremamente poderosa.[16]
Remove ads
Ver também
Referências
- Verevkin, A.; Pearlman, A.; Slstrokysz, W.; Zhang, J.; Currie, M.; Korneev, A.; Chulkova, G.; Okunev, O.; Kouminov, P.; Smirnov, K.; Voronov, B.; N. Gol'tsman, G.; Sobolewski, Roman (2004). "Ultrafast superconducting single-photon detectors for near-infrared-wavelength quantum communications". Journal of Modern Optics 51 (12): 1447–1458. doi:10.1080/09500340410001670866.
- LCWU Online Course Directory https://ocd.lcwu.edu.pk › cfilesPDF Decaborane (B10H14)
- Verevkin, A.; Pearlman, A.; Slstrokysz, W.; Zhang, J.; Currie, M.; Korneev, A.; Chulkova, G.; Okunev, O.; Kouminov, P.; Smirnov, K.; Voronov, B.; N. Gol'tsman, G.; Sobolewski, Roman (2004). "Ultrafast superconducting single-photon detectors for near-infrared-wavelength quantum communications". Journal of Modern Optics 51 (12): 1447–1458. doi:10.1080/09500340410001670866.
- Gary B. Dunks, Kathy Palmer-Ordonez, Eddie Hedaya "Decaborane(14)" Inorg. Synth. 1983, vol. 22, pp. 202–207. doi:10.1002/9780470132531.ch46
- Charles R. Kutal; David A. Owen; Lee J. Todd (1968). «closo -1,2-Dicarbadodecaborane(12): [ 1,2-Dicarbaclovododecaborane(12 )]». Inorganic Syntheses. 11. [S.l.: s.n.] pp. 19–24. ISBN 978-0-470-13170-1. doi:10.1002/9780470132425.ch5
- M. Frederick Hawthorne; Timothy D. Andrews; Philip M. Garrett; Fred P. Olsen; Marten Reintjes; Fred N. Tebbe; Les F. Warren; Patrick A. Wegner; Donald C. Young (1967). «Icosahedral Carboranes and Intermediates Leading to the Preparation of Carbametallic Boron Hydride Derivatives». Inorganic Syntheses. 10. [S.l.: s.n.] pp. 91–118. ISBN 978-0-470-13241-8. doi:10.1002/9780470132418.ch17
- RSC Publishing https://pubs.rsc.org › articlelanding The synthesis and topochemical polymerization of o-carborane-based ...
- UNL Digital Commons https://digitalcommons.unl.edu › ...PDF Deposition of Boron-Containing Films From Decaborane - UNL Digital Commons
- Nakano, T.; Higashijima, S.; Kubo, H.; Yagyu, J.; Arai, T.; Asakura, N.; Itami, K. «Boronization effects using deuterated-decaborane (B10D14) in JT-60U». 15th PSI Gifu, P1-05. Sokendai, Japan: National Institute for Fusion Science. Cópia arquivada em 30 de maio de 2004
- Jong Woo Bae; Seung Hwan Lee; Young Jin Cho; Cheol Min Yoon (2000). «A reductive amination of carbonyls with amines using decaborane in methanol». J. Chem. Soc., Perkin Trans. 1 (2): 145–146. doi:10.1039/A909506C
- National Institutes of Health (NIH) (.gov) https://pubmed.ncbi.nlm.nih.gov › ... Decaborane: From Alfred Stock and Rocket Fuel Projects to Nowadays
- ScienceDirect.com https://www.sciencedirect.com › pii Fuel cell power source based on decaborane with high energy density and low crossover
- National Institutes of Health (NIH) (.gov) https://pubchem.ncbi.nlm.nih.gov › ... Solid propellant and process using vinyl decaborane compounds
- «The Most DESTRUCTIVE Chemical Reaction from two NON-explosive components». YouTube. 21 December 2023.
YouTube video name: 'The Most DESTRUCTIVE Chemical Reaction from two NON-explosive components'
Verifique data em:|data=(ajuda)
Remove ads
Leitura posterior
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads