Лучшие вопросы
Таймлайн
Чат
Перспективы
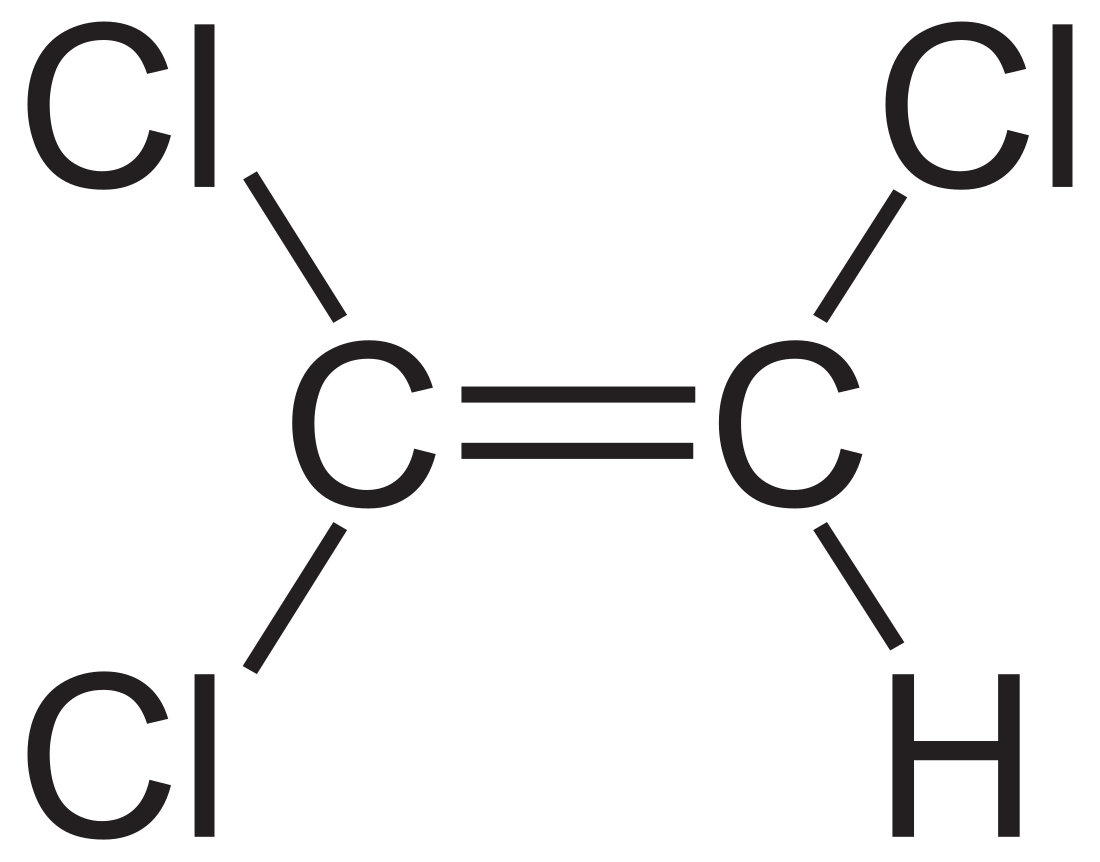
Трихлорэтилен
химическое соединение Из Википедии, свободной энциклопедии
Remove ads
Трихлорэтилен (Trichloraetylenum), трихлорэтен — хлорорганическое соединение, бесцветная, прозрачная, подвижная, летучая жидкость со сладким запахом, напоминающим запах хлороформа, и сладким, жгучим вкусом. Приблизительно в полтора раза плотнее воды.
Хорошо смешивается с органическими растворителями. Практически нерастворим в воде.
Трудногорюч (в нормальных условиях не воспламеняется и не взрывается).
Под действием света и воздуха разлагается с образованием фосгена и галогенсодержащих кислот, при этом приобретает розовое окрашивание. Для стабилизации трихлорэтилена к нему добавляют 0,01 % тимола или 0.001% фенола.
Наркотик, токсичен.
Трихлорэтилен используется в промышленности в качестве растворителя и сырья для органического синтеза.
Remove ads
Физические свойства
В нормальных условиях трихлорэтилен находится в жидкой фазе. Замерзает при −73 °C, кипит при 86,7 °C[3].
Относительная плотность 1,462—1,466, 1,4642[3].
Теплопроводность жидкости: 0,142 Вт/м·К при −40 °C, 0,138 Вт/м·К при 20 °C, 0,099 Вт/м·К при 80 °C[3]. Теплопроводность пара: 0,00833 Вт/м·К при 86,7 °C[3].
Трихлорэтилен с водой образует азеотропную смесь с температурой кипения 73 °C (73 % трихлорэтилена, 7 % воды). В воде плохо растворяется, массовая доля в растворе от 0,017 % до 0,125 % в диапазоне температур 10—60 °C[3].
Remove ads
Химические свойства
Трихлорэтилен нельзя хранить на свету, так как в присутствии кислорода воздуха он разлагается с образованием токсичного (и воспламеняющегося) продукта — дихлорацетилена, который, в свою очередь, разлагается на фосген, угарный газ и хлороводород. Реакцию катализируют пары йода, минеральные кислоты и натронная известь.[источник не указан 1959 дней]
При окислении трихлорэтилена озоном образуются фосген, хлористый водород и оксиды углерода[4].
При окислении трихлорэтилена кислородом образуется окись трихлорэтилена и дихлорацетилхлорид[5].
В присутствии катализаторов и при высоких температурах может образовывать другие хлорорганические соединения, чаще предельного строения.
В присутствии хлорида алюминия трихлорэтилен взаимодействует с хлороводородом, при этом происходит конденсация, полимеризация и осмоление[3].
Взаимодействует с фтором, хлором, бромом с образованием 1,2-дигалоген-1,2,2-трихлорэтанов. При хлорировании превращается в пентахлорэтан. С йодом не реагирует[6].
Remove ads
Получение
Трихлорэтилен получают путём каталитического высокотемпературного хлорирования отходов производства винилхлорида или дихлорэтана (смесь хлорэтанов и хлорэтиленов). Также получают из дихлорэтана и других отдельных соединений. Температуры каталитического хлорирования — от 350° до 450 °С в зависимости от состава сырья и катализатора[3].
Применение
Являясь хорошим растворителем, трихлорэтилен широко применяется в промышленности и быту. Используется для улучшения свойств инсектицидов[7]. Применяется для обезжиривания металлов, для химической чистки тканей[3].
Используется в органическом синтезе для очистки полученных веществ и в качестве полупродукта. Добавляется в инсектициды для улучшения их свойств. Используется при синтезе лекарств, например, является промежуточным продуктом при синтезе левомицетина[7].
На основе трихлорэтилена разработаны удобные процессы получения разнообразных веществ. С его помощью изготавливают пестициды и инсектициды, среди его производных — огнезащитные агенты, пламегасители, регуляторы молекулярного веса в производстве синтетических материалов, полилактоны[7].
Remove ads
Биологическое действие
Суммиров вкратце
Перспектива
Трихлорэтилен является токсичным наркотическим веществом. Накапливается в организме, представляет опасность для сердечно-сосудистой и нервной систем, органов дыхания, зрения. При продолжительном воздействии на кожу вызывает её повреждение и дерматиты[8].
Трихлорэтилен до 500 % повышает риск развития болезни Паркинсона[9]
В организм человека трихлорэтилен, помимо проглатывания, может попадать при дыхании, проникает через кожу[8].
Предельно допустимая концентрация (ПДК) паров трихлорэтилена в атмосферном воздухе 1 мг/м³ (максимальная разовая — 4 мг/м³). Имеет третий класс опасности по ГОСТ 12.1.005. ПДК в воде — 0,06 мг/дм³[8].
По данным[10] ПДК в воздухе рабочей зоны равна 10 мг/м3 среднесменная и 30 мг/м3 максимально разовая. Порог восприятия запаха может достигать 538 мг/м3[11] и 440—580 мг/м3[12]. Соответственно, замена противогазных фильтров у СИЗОД по ощущению появления запаха в маске (как это советуют поставщики респираторов) приведёт к тому, что хотя бы часть работников будет менять фильтры запоздало. Необходимо использовать современные безопасные способы[13].
Ранее трихлорэтилен применялся для наркоза и обезболивания в качестве ингаляционного анестетика[6][14]. В большинстве стран, в том числе в России, в этом качестве ныне не используется[14].
Ототоксичен (может ухудшать слух)[15][16].
Remove ads
Хранение
Трихлорэтилен хранится в сухом, прохладном, защищённом от света месте.[источник не указан 1959 дней]
Примечания
Литература
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads