
Глутатион
трипептид γ-глутамилцистеинилглицин / Материал из Википедии — свободной encyclopedia
Глутатион (2-амино-5-{[2-[(карбоксиметил)амино]-1-(меркаптометил)-2-оксоэтил]амино}-5-оксопентаноевая кислота, англ. glutathione, GSH) — это трипептид γ-глутамилцистеинилглицин. Глутатион содержит необычную пептидную связь между аминогруппой цистеина и карбоксильной группой боковой цепи глутамата. Значение глутатиона в клетке определяется его антиоксидантными свойствами. Фактически глутатион не только защищает клетку от токсичных свободных радикалов, но и в целом определяет окислительно-восстановительные характеристики внутриклеточной среды[1].
| Глутатион | |
|---|---|
 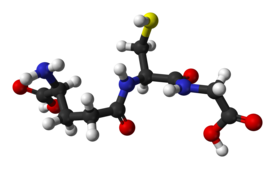  | |
| Общие | |
| Систематическое наименование |
(2S)-2-Amino-4-'"`UNIQ--nowiki-00000000-QINU`"'{[(1R)-1-[(carboxymethyl)carbamoyl]-2-sulfanylethyl]carbamoyl}butanoic acid |
| Хим. формула | C10H17N3O6S |
| Физические свойства | |
| Молярная масса | 307.32 г/моль |
| Классификация | |
| Рег. номер CAS | 70-18-8 |
| PubChem | 124886 |
| Рег. номер EINECS | 200-725-4 |
| SMILES | |
| InChI | |
| ChEBI | 16856 |
| ChemSpider | 111188 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
В клетке тиоловые группы находятся в восстановленном состоянии (SH). Концентрация глутатиона в клетке составляет около 5 мМ. Фактически такая высокая концентрация глутатиона в клетке приводит к тому, что он восстанавливает любую дисульфидную связь (S-S), образующуюся между остатками цистеина внутриклеточных белков. При этом восстановленная форма глутатиона GSH превращается в окисленную GSSG. Восстанавливается окисленный глутатион под действием фермента глутатионредуктазы, который постоянно находится в клетке в активном состоянии и индуцируется при окислительном стрессе. Соотношение восстановленной и окисленной форм глутатиона в клетке является одним из важнейших параметров, который показывает уровень окислительного стресса.