
Hlorna kiselina
From Wikipedia, the free encyclopedia
Hlorna kiselina je veoma jaka neorganska kiselina. Hlorna kiselina je bezbojna, nepostojana tečnost gustine 1,28 g/cm³. Njena molekulska formula je HClO3. Ona je jako oksidaciono sredstvo. Njena temperatura topljenja je ispod -20 °C, a na temperaturi 40 °C podleže raspadu. Najlakše se dobija dodavanjem sumporne kiseline u vodeni rastvor barijum hlorata (tada se izdvaja nerastvorljiv barijum sulfid).
- Ba(ClO3)2 + H2SO4 → 2HClO3 + BaSO4
Quick Facts Identifikacija, Svojstva ...
| Hlorna kiselina | |
|---|---|
 | |
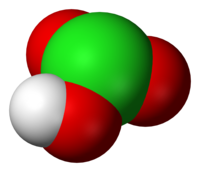 | |
| Drugi nazivi | Hlorna(V) kiselina |
| Identifikacija | |
| CAS registarski broj | 7790-93-4 |
| ChemSpider[1] | 18513 |
| MeSH | Chloric+acid |
| Jmol-3D slike | Slika 1 |
| Svojstva | |
| Molekulska formula | HClO3 |
| Molarna masa | 84.45914 g mol−1 |
| Agregatno stanje | bezbojan rastvor |
| Gustina | 1 g/mL, rastvor (aproksimativno) |
| Rastvorljivost u vodi | >40 g/100 ml (20 °C) |
| pKa | ca. −1 |
| Struktura | |
| Oblik molekula (orbitale i hibridizacija) | trigonalna piramida |
| Opasnost | |
| Opasnost u toku rada | Oksidant |
| Srodna jedinjenja | |
| Drugi anjoni | bromna kiselina jodna kiselina |
| Drugi katjoni | amonijum-hlorat natrijum-hlorat kalijum-hlorat |
| Srodna jedinjenja | hlorovodonična kiselina hipohlorasta kiselina hlorasta kiselina perhlorna kiselina |
|
| |
| Infobox references | |
Close
Drugi metod je zagrevanje hipohloraste kiseline, iz koje se formiraju hlorna kiselina i hlorovodonik:
- 3HClO → HClO3 + 2 HCl
Spada u kiseonične kiseline hlora.