Koordinacijska geometrija
From Wikipedia, the free encyclopedia
Remove ads
{glavni|Kompleksna spojina}} Izraz koordinacijska geometrija se uporablja na številnih sorodnih področjih kemije in kemije/fizike trdne snovi.
Molekule
Koordinacijska geometrija molekul je geometrijska oblika, ki jo tvorijo atomi, vezani okrog centralnega atoma.
Anorganski koordinacijski kompleksi
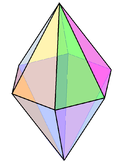
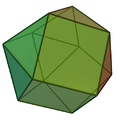
V anorganskih koordinacijskih kompeksih tvorijo geometrijske vzorce atomi ligandov, ki so vezani na centralni atom molekule. Geometrijska razporeditev atomov je odvisna od števila in vrste ligandov in koordinacijskih prioritet centralnega atoma, ki je običajno kovina. Število vezanih atomov, se pravi število σ-vezi med centralnim atomom in ligandi, je koordinacijsko število. Geometrijski vzorec se lahko prikaže kot polieder, katerega oglišča so središča koordiniranih atomov v ligandih.[1]
Koordinacijska prioriteta centralnega atoma se pogosto spreminja z njegovim oksidacijskim stanjem. Število koordiniranih vezi (koordinacijsko število) lahko variira od 2 do 20 v Th(η5-C5H5)4.[2]
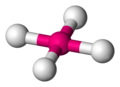
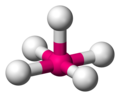
Ena od najbolj pogostih koordinacijskih geometrij je oktaeder, v katerem je šest ligandov koordiniranih na kovino v simetrični porazdelitvi. Če se središča ligandov povežejo s črtami, dobi molekula obliko oktaedra. Drugi pogosti koordinacijski geometriji sta tetraedska in kvadratno planarna.
Za razlago relativnih stabilnosti spojin prehodnih kovin z različnimi koordinacijskimi geometrijami, pa za tudi prisotnost ali odsotnost paramagnetizma, se lahko uporabi teorijo kristalnega polja.
Za napovedovanje geometrije kompleksov elementov iz glavnih skupin periodnega sistema se lahko uporabi tudi teorijo o odboju valenčnih elektronskih parov.
Remove ads
Kristalografija
Koordinacijska geometrija atomov v kristalni strukturi je geometrijski vzorec koordiniranih atomov, pri čemer je definicija koordiniranih atomov odvisna od uporabljenega modela.[1] V kuhinjski soli, na primer, je vsak natrijev atom obdan s po šestimi atomi klora v obliki oktaedra. V kovinskih kristalih s telesno centrirano kocko je vsak atom obdan z osmimi najbližjimi sosedi v obliki kocke. V kovinskih kristalih s ploskovno centrirano kocko je vsak atom obdan z dvanajstimi najbližjimi sosedi v kubično tetraedrski obliki.
Pregled geometrijskih oblik
V preglednici so prikazane geometrijske oblike in primeri kompleksov, v katerih se te oblike pojavljajo. V nediskretnih kompleksih so spojine in koordinacijske sfere prikazane v diskretnih enotah.
Remove ads
Poimenovanje anorganskih spojin
IUPAC je v svojem priporočilu za nomenklaturo anorganskih spojin leta 2005 uvedel poliedrski simbol,[6] ki opisuje geometrijo okrog centralnega atoma v spojini.
IUCr je predlagal simbol, ki je v kemijski formuli zapisan kot eksponent v oglatih oklepajih. Primer: CaF2 se zapiše kot Ca[8cb]F2[4t]. Zapis [8cb] pomeni kubično koordinacijo, [4t] pa tetraeder. Enakovredna zapisa IUPAC sta CU-8 in T-4.[6] IUPACovi simboli so primerni za kompleksne spojine in molekule, IUCrjevi pa za kristalinične trdne snovi.
Remove ads
Sklici
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads