From Wikipedia, the free encyclopedia
Хибридизација је концепт мешања атомских орбитала при чему се формирају нове хибридне орбитале.[1] Хибридне орбитале су корисне за објашњење и описивање геометријског облика молекула.[2][3]
При мијешању и орбитала, долази до помијерања центра наелектрисања електронског облака у односу на орбиталу.
Теорију хибридизације је први предложио хемичар Линус Паулинг како би објаснио структуру молекула као што је метан.[4] Према теорији и методи валентне везе, геометријски облик молекула и усмјереност веза у простору посљедица је преклапања атомских орбитала које је утолико повољније уколико може достићи максималну вриједност. Полазећи од електронске конфигурације некада је тешко објаснити усмјереност веза у простору. За описивање структуре таквих молекула користи се концепт хибридизације. Хибридизација није неопходна за описивање свих молекула, него углавном налази примјену за описивање геометријског облика молекула који садрже угљеник, азот, кисеоник и фосфор.
Хибридизација према броју модификованих атомских орбитала у угљениковом атому може бити:
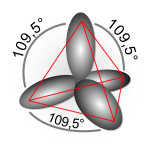
Примјер 3 хибридизације је молекул метана , који има тетраедарски облик.
Атом угљеника у основном стању има конфигурацију:
Од четири валентна електрона угљеника два се налазе под правим углом(у двије орбитале) а друга два се налазе у орбитали те немају никакво усмјерење у простору, док су у молекулу метана валенце метана усмјерене тетраедарски у простору.
Угљеников атом при сједињавању најприје прелази у стање промоције (тј. један електрон прелази у празну орбиталу):
Након тога долази до хибридизације, тј. до укрштања или мијешања једне и три орбитале (). При томе настају четири једнаке орбитале усмјерене ка тјеменима тетраедра у простору. Ове орбитале се називају 3 орбитале.
Прецизније речено 3 хибридне орбитале се добију на основу рјешења Шредингерове једначине за конфигурацију електрона у побуђеном стању[5], тј. након промоције и представљају линерарну комбинацију и орбитала.[6]
Везивањем са четири атома водоника (преклапањем 3 хибридних орбитала угљеника са орбиталама водоника при чему се стварају четири сигма везе) настаје молекул метана који има тетраедарски облик. 3 хибридизација је карактеристична за засићене угљоводонике.
До 3 хибридизације долази и код атома кисеоника и азота у молекулу воде и амонијака. При томе у молекулу воде двије 3 хибридне орбитале су преклопљене са орбиталама два атома водоника(тј. успостављена је хемијска веза) а двије 3 хибридне орбитале садрже два слободна електронска пара. Код молекула амонијака једна 3 хибридна орбитала садржи слободан електронски пар. Слободни електронски парови се одбијају, а дјелују и на електроне у преосталим хибридним орбиталама због чега долази до смањивања угла између веза.

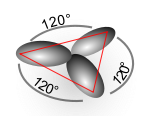
Примјер 2 хибридизације је молекул етена, који садржи двоструку везу између два атома угљеника. У молекулу етена су 2 хибридизована оба атома угљеника. Код атома угљеника долази до мијешања орбитале са двије орбитале, при чему се добију три 2 хибридне орбитале које се налазе у истој равни а угао између њих је 120° степени. Такође је остала и једна орбитала која није хибридизована.
У молекулу етена два атома угљеника се међусобно спајају сигма ковалентном везом која настаје преклапањем двије 2 орбитале и сваки атом угљеника ствара двије сигма везе са по два атома водоника преклапањем 2 орбитале угљеника и орбитале водоника. Такође се између два атома угљеника формира π веза бочним преклапањем двије орбитале које су нормалне на раван молекула.
До хибридизације долази код алкина који садрже троструку везу између два атома угљеника. У овом случају орбитала се мијеша само са једном орбиталом при чему настају двије орбитале између којих је угао од 180° степени и остају двије орбитале које су непромијењене.
У молекулу етина између два атома угљеника настаје једна сигма веза преклапањем и двије додатне π везе које се добију бочним преклапањем орбитала. Сваки атом угљеника ствара и једну сигма везу са атомом водоника преклапањем.
Хибридизација може објаснити облике молекула:
Ако на централном атому има слободних електронских парова онда углови између веза постају мањи због повећаног одбијања. На примјер у молекулу воде на атому кисеоника постоје двује везе са атомима водоника и два слободна електронска пара. Модел молекула је онда и долази до 3 хибридизације и распоред електронских парова у молекулу воде је тетраедарски. Угао између веза је 104.5°.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.