Топ питань
Часова шкала
Чат
Перспективи
Період 3 періодичної системи елементів
З Вікіпедії, вільної енциклопедії
Remove ads
До третього періоду періодичної системи відносяться елементи третього рядка (або третьої періоду) періодичної системи хімічних елементів. Будова періодичної таблиці заснована на рядках для ілюстрації повторюваних (періодичних) трендів у хімічних властивостях елементів при збільшенні атомного номера: новий рядок починається тоді, коли хімічні властивості повторюються, що означає, що елементи з аналогічними властивостями потрапляють в один і той же вертикальний стовпець. Усі атоми третього періоду періодичної системи мають три електронні оболонки. Зовнішня (третя) електронна оболонка може бути занята від одного до максимально восьми електронів (аргон - [Ne] 3s2 3p6). Таким чином третій період містить 8 хімічних елементів (як і попередній), до нього входять: натрій, магній, алюміній, кремній, фосфор, сірка, хлор і аргон. Перші два з них, натрій і магній, входять до s-блоку періодичної таблиці, тоді як інші відностяться до р-блоку. Слід звернути увагу, що 3d-орбіталі у елементів не заповнені до 4 періоду, що дає періодам таблиці їх характерний вигляд «два рядки в одному».
| Третій період періодичної системи |
Remove ads
Огляд
Всі елементи третього періоду зустрічаються в природі і мають принаймні один стабільний ізотоп.
Елементи
Узагальнити
Перспектива
| Група | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| I | II | III | IV | V | VI | VII | VIII | |||||||||||
| Символ | 11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar | ||||||||||
| Лужні метали | Лужноземельні метали | Лантаноїди | Актиноїди | Перехідні метали | Постперехідні метали | напівметали | Неметали | Галогени | Інертні гази |
Електронні конфігурації
Хімічний елемент Група періодичної системи Електронна конфігурація 11 Na Натрій Лужний метал [Ne] 3s1 12 Mg Магній Лужноземельний метал [Ne] 3s2 13 Al Алюміній Постперехідний метал [Ne] 3s2 3p1 14 Si Кремній Металоїд [Ne] 3s2 3p2 15 P Фосфор Неметал [Ne] 3s2 3p3 16 S Сірка Неметал [Ne] 3s2 3p4 17 Cl Хлор Галоген [Ne] 3s2 3p5 18 Ar Аргон Інертний газ [Ne] 3s2 3p6
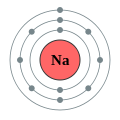
Натрій

Натрій (Na) — лужний метал сріблясто-білого кольору з атомним номером 11, атомною масою 22,98977, що має один стабільний ізотоп 23Na.
Вміст натрію у земній корі 2,64% за масою. Натрій присутній у великих кількостях у світовому океані у формі хлориду натрію. У живих організмах натрій знаходиться більшою частиною зовні клітин (приблизно у 15 разів більше ніж у цитоплазмі). Цю різницю підтримує натрій-калієвий насос, який відкачує натрій, що потрапив всередину клітини. Рекомендована доза натрію становить для дітей від 600 до 1700 міліграмів, для дорослих від 1200 до 2300 міліграмів. У вигляді кухонної солі це становить від 3 до 6 грамів на день.
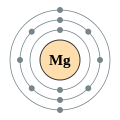
Магній

Магній (Mg) — лужноземельний метал сріблясто-білого кольору з атомним номером 12 і атомною масою 24,305. Має три стабільних ізотопи: 24Mg (78,60%), 25Mg (10,11%), 26Mg (11,29%).
Основна область використання магнію — виробництво магнієвих сплавів. Магній застосовують також для легування сплавів на основі алюмінію, для металотермічного отримання деяких металів (Ti, U, Zr, V та ін.), для розкислення та десульфурації ряду металів і сплавів, у синтезі магнійорганічних з'єднань. Йони магнію знайдені у хлорофілі.
Алюміній

Алюміній (Al) — постперехідний метал сріблясто-білого кольору з атомним номером 13, атомною масою 26,98154, що має один стабільний ізотоп 27Al.
Вміст алюмінію у земній корі 8,8% за масою. За поширеністю у природі він займає четверте місце серед всіх елементів (після кисню, водню і кремнію) та перше серед металів. У вільному вигляді не зустрічається. Алюміній використовують головним чином для отримання алюмінієвих сплавів. Чистий алюміній — конструкційний матеріал у будівництві будинків, у суднобудуванні, для обладнання силових підстанцій і т. д. Застосовують алюміній також для виготовлення кабельних, струмопровідних та інших виробів в електротехніці, корпусів і охолоджувачів діодів, спеціальної хімічної апаратури, товарів народного споживання. Покриття з алюмінію наносять на сталеві вироби для підвищення їх корозійної стійкості.
Кремній

Кремній (Si) — металоїд, напівпровідник з атомним номером 14. Чиста речовина утворює темно-сірі зі смолистим блиском крихкі кристали з гранецентрованою кубічною ґраткою типу алмазу. За новою номенклатурою IUPAC Силіцій належить до групи 14 періодичної системи елементів, за старою — до IV підгрупи основної групи.
Густина кремнію 2,328, tплав 1415 °C, tкип 3250 °C. Твердість за Брінеллем 2,4 ГПа, за Моосом 7. Модуль пружності 109 ГПа. Кремній — напівпровідник, електричні властивості якого сильно залежать від домішок.
При низькій температурі Силіцій хімічно інертний. З багатьма металами утворює силіциди. Вміст у земній корі 27,6% за масою. Солі кремнієвих кислот поширені в природі — мінерали класу природних силікатів. При ізоморфному заміщенні в їхній структурі частини кремнію алюмінієм утворюються алюмосилікати. Відомо понад 400 мінералів, що містять Силіцій. Найважливіші мінерали Силіцію — силікати, кремнезем.
На кремнію виготовляють більшість інтегральних схем.
Фосфор

Фосфор (P) — хімічний елемент 15-ї групи (по застарілої класифікації — головної підгрупи п'ятої групи) третього періоду періодичної системи; неметал; має атомний номер 15. Один з поширених елементів земної кори: його зміст становить 0,08-0,09% її маси. Концентрація у морській воді 0,07 мг/л[1]. У вільному стані не зустрічається через високу хімічну активность. Утворює близько 190 мінералів, найважливішими з яких є апатит Ca 5 (PO 4 ) 3 (F, Cl, OH), фосфорит та інші. Фосфор міститься у всіх частинах зелених рослин, ще більше його в плодах і насінні (див. фосфоліпіди). Міститься в тканинах тварин, входить до складу білків та інших найважливіших органічних сполук (АТФ, ДНК), є елементом життя.
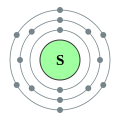
Сірка

Сірка (S) — хімічний елемент VI групи періодичної системи елементів, неметал, атомова вага 32,064; неметал; жовта кристалічна речовина. Досить поширений елемент, на неї припадає близько 0,1% маси земної кори. У природі вона зустрічається як у вільному стані — так звана самородна сірка, але значно частіше сірка зустрічається у зв'язаному вигляді, тобто у вигляді різних сполук. Найважливіші з них — залізний колчедан, або пірит FeS2, цинкова обманка ZnS, свинцевий блиск PbS, мідний блиск Cu2S, гіпс CaSO4 · 2H2O, мірабіліт Na2SO4 · 10H2O тощо.
У невеликих кількостях сірка міститься в кам'яному вугіллі і нафті, а також в усіх рослинних і тваринних організмах, оскільки вона входить до складу білків. Знайдена у двох амінокислотах: цистеїні та метіоніні.
Сірку застосовують переважно у хімічній промисловості для виробництва сірчаної кислоти, синтетичного волокна, сірчистих барвників, димного пороху, у ґумовій промисловості, також у сільському господарстві, фармацевтиці тощо.
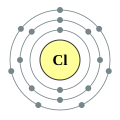
Хлор

Хлор (Cl) — елемент 17-ї групи періодичної таблиці хімічних елементів (за застарілою класифікацією — елемент головної підгрупи VII групи) з атомним номером 17[2]. Позначається символом Cl (лат. Chlorum). Хімічно активний неметал. Входить у групу галогенів (спочатку назву «галоген» використовував німецький хімік Швейгер для хлору [дослівно «галоген» перекладається як солерід], але воно не прижилося, і згодом стало загальним для VII групи елементів, у яку входить і хлор[3]).
Проста речовина хлор (CAS-номер: 7782-50-5) за нормальних умовах — отруйний газ жовтувато-зеленого кольору важчий за повітря, з різким запахом. Молекула хлору двоатомна (формула Cl 2). Використовується як дезинфікуючий засіб, особливо у плавальних басейнах.
Аргон

Аргон (Ar) є інертним газом, що робить його майже повністю нереакціонноспособним. Лампи розжарювання часто заповнюють інертними газами, у тому числі і аргоном, що оберігає нитки від перегорання при високих температурах.
хімічний елемент з атомним номером 18, а також його проста речовина, інертний газ, без кольору і запаху. Вважається, що він не вступає в реакції з іншими елементами, проте недавно встановлено, що він може з'єднуватися з фторидом бору. Міститься в атмосфері Землі (1 %).
Відноситься до нульової групи періодичної системи елементів, атомна вага 39,944. Природний аргон складається з ізотопів 36Ar (0,337%). 38Ar (0,063%), 40Ar (99,600%); штучно одержано радіоактивні ізотопи 35Ar, 37Ar і 41Ar.
Аргон — безколірний, молекули його одноатомні; t° кип. — 185,83 °C, t° плав.— 189,3 °C, критична температура — 122,4 °C; критичний тиск — 48 атм. В природі аргон зустрічається лише у вільному стані і становить 0,933% (за об'ємом) повітря, з якого вперше його виділили у 1894 році У. Рамзай і Дж. Релей. У промисловості аргон добувають фракціонуванням рідкого повітря.
Remove ads
Примітки
Література
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads