Топ питань
Часова шкала
Чат
Перспективи
Гліцеральдегід-3-фосфатдегідрогеназа
білок людини З Вікіпедії, вільної енциклопедії
Remove ads
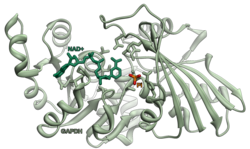
Гліцеральдегід-3-фосфатдегідрогеназа (англ. Glyceraldehyde-3-phosphate dehydrogenase) – білок, який кодується геном GAPDH, розташованим у людей на короткому плечі 12-ї хромосоми. [3] Довжина поліпептидного ланцюга білка становить 335 амінокислот, а молекулярна маса — 36 053[4].
Послідовність амінокислот
| 10 | 20 | 30 | 40 | 50 | ||||
| MGKVKVGVNG | FGRIGRLVTR | AAFNSGKVDI | VAINDPFIDL | NYMVYMFQYD | ||||
| STHGKFHGTV | KAENGKLVIN | GNPITIFQER | DPSKIKWGDA | GAEYVVESTG | ||||
| VFTTMEKAGA | HLQGGAKRVI | ISAPSADAPM | FVMGVNHEKY | DNSLKIISNA | ||||
| SCTTNCLAPL | AKVIHDNFGI | VEGLMTTVHA | ITATQKTVDG | PSGKLWRDGR | ||||
| GALQNIIPAS | TGAAKAVGKV | IPELNGKLTG | MAFRVPTANV | SVVDLTCRLE | ||||
| KPAKYDDIKK | VVKQASEGPL | KGILGYTEHQ | VVSSDFNSDT | HSSTFDAGAG | ||||
| IALNDHFVKL | ISWYDNEFGY | SNRVVDLMAH | MASKE |
Цей білок за функціями належить до оксидоредуктаз, трансфераз. Задіяний у таких біологічних процесах як апоптоз, гліколіз, регуляція трансляції. Білок має сайт для зв'язування з НАД. Локалізований у цитоплазмі, цитоскелеті, ядрі, мембрані.
Remove ads
Участь у гліколізі
Узагальнити
Перспектива

Гліцеральдегід-3-фосфатдегідрогеназа каталізує реакцію окиснення гліцеральдегід-3-фосфату із одночасним його фосфорилюванням. Це перша реакція гліколізу в якій виділяється енергія. В ході цієї реакції альдегід перетворюється не на вільну кислоту, а на змішаний ангідрид із фосфатною кислотою (1,3-бісфосфогліцерат). Сполуки такого типу — ацилфосфати — мають дуже велику від'ємну зміну вільної енергії гідролізу (ΔG0 = −49,3 кДж/моль)[5].
Реакцію перетворення гліцеральдегід-3-фосфату в 1,3-бісфосфогліцерат можна розглядати як два окремі процеси: окиснення альдегідної групи за допомогою НАД+ та приєднання фосфатної групи до утвореної карбонової кислоти. Перша реакція термодинамічно вигідна (ΔG0 = −50 кДж/моль), друга, навпаки, невигідна. Зміна вільної енергії для другої реакції майже така сама, тільки ця зміна додатна. Якби вони відбувались послідовно одна за одною, то друга реакція вимагала б надто великої енергії активації, щоб перебігати в клітині з достатньою швидкістю. Але обидва процеси є спряженими тому, що проміжна сполука — 3-фосфогліцерат — ковалентно зв'язана із залишком цистеїну тіоестерним зв'язком в активному центрі ферменту. Такий тип зв'язку дозволяє «законсервувати» частину енергії, яка виділяється під час окиснення гліцеральдегід-3-фосфату, та використати її для реакції із ортофосфатною кислотою[6].
Remove ads
Примітки
Література
Див. також
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads