
Метан
найпростіша органічна сполука вуглецю з воднем / З Вікіпедії, безкоштовно encyclopedia
Шановний Wikiwand AI, Давайте зробимо це простіше, відповівши на ключові запитання:
Чи можете ви надати найпопулярніші факти та статистику про Метан?
Підсумуйте цю статтю для 10-річної дитини
Мета́н (англ. methane, нім. Methan n) — найпростіша органічна сполука вуглецю з воднем, природний безбарвний газ без запаху, хімічна формула — CH4.
| Метан | |
|---|---|
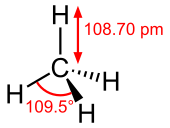 Стерео, скелетна формула метану з доданими вимірами | |
 Модель метану з кульок і паличок |
 Компактна модель метану |
| Систематична назва | Carbane (не рекомендується ніколи[1]) |
| Інші назви |
|
| Ідентифікатори | |
| Номер CAS | 74-82-8 |
| PubChem | 297 |
| Номер EINECS | 200-812-7 |
| DrugBank | 15994 |
| KEGG | C01438 |
| Назва MeSH | Methane |
| ChEBI | 16183 |
| RTECS | PA1490000 |
| SMILES | C |
| InChI | InChI=1S/CH4/h1H4 |
| Номер Бельштейна | 1718732 |
| Номер Гмеліна | 59 |
| 3DMet | B01453 |
| Властивості | |
| Молекулярна формула | CH4 |
| Молярна маса | 16,04 г/моль |
| Зовнішній вигляд | безбарвний газ |
| Запах | без запаху |
| Густина | |
| Тпл | -182.456 |
| Розчинність (вода) | 22.7 mg·L−1[4] |
| Розчинність | розчинний в етанолі, діетиловому етері, бензені, толуені, метанолі, ацетоні і нерозчинний у воді |
| Структура | |
| Геометрія | тетраедр |
| Дипольний момент | 0 D |
| Термохімія | |
| Ст. ентальпія утворення ΔfH 298 |
−74.6 kJ·mol−1 |
| Ст. ентальпія згоряння ΔcH 298 |
−891 kJ·mol−1 |
| Ст. ентропія S 298 |
186.3 J·(K·mol)−1 |
| Теплоємність, c p |
35.7 J·(K·mol)−1 |
| Небезпеки | |
| ГГС піктограми |  |
| ГГС формулювання небезпек | 220 |
| ГГС запобіжних заходів | 210 |
| NFPA 704 | |
| Вибухові границі | 4.4–17 % |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |

Метан є основною складовою природного газу. Крім того, він міститься в кам'яновугільних пластах — під час їхньої розробки утворюються вибухонебезпечні суміші метану з повітрям, так званий «рудниковий газ».
Зустрічається в осадовому чохлі земної кори у вигляді вільних скупчень (покладів), в розчиненому (в нафті, пластових і поверхневих водах), розсіяному, сорбованому (породами і органічною речовиною) і твердому (газогідратному) станах.
При використанні в побуті, до метану звичайно додають одоранти зі специфічним «запахом газу».
