Fluor nitrat hay còn được gọi là flo nitrat, là một dẫn xuất không bền của acid nitric với công thức FNO
3. Nó khá nhạy cảm với một cú sốc.[1] Do tính không ổn định của hợp chất này, nó thường được sản xuất từ chlor nitrat khi cần thiết.[cần dẫn nguồn].
Thông tin Nhanh Nhận dạng, Số CAS ...
| Fluor nitrat |
|---|
 |
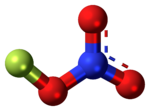 |
|
| Nhận dạng |
|---|
| Số CAS | 7789-26-6 |
|---|
| PubChem | 123262 |
|---|
| Ảnh Jmol-3D | ảnh |
|---|
| SMILES | |
|---|
| UNII | 1Q6BYH7F2B |
|---|
| Thuộc tính |
|---|
| Khối lượng riêng | 2.217 g/L[1] |
|---|
| Điểm nóng chảy | −175 °C (98,1 K; −283,0 °F) |
|---|
| Điểm sôi | −46 °C (227 K; −51 °F) |
|---|
| Nhiệt hóa học |
|---|
Enthalpy
hình thành ΔfHo298 | +10.46 kJ/mol |
|---|
| Các nguy hiểm |
|---|
| Nguy hiểm chính | Khí gây nổ |
|---|
|
|
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). |
Đóng
Điều chế
Fluor nitrat được tạo thành khi khí fluor phản ứng acid nitric hoặc với muối kali nitrat rắn:[2]


Tính chất
Fluor nitrat phản ứng với nước để tạo thành khí oxy, acid hydrofloric và acid nitric:[1]

Ruff, Otto; Kwasnik, Walter (1935). “The fluorination of nitric acid. The nitroxyfluoride, NO3F”. Angewandte Chemie. 48: 238–240. doi:10.1002/ange.19350481604. Yost, Don M.; Beerbower, Alan. “The Reaction of Fluorine with Nitric acid and with Solid Potassium Nitrate to Form NO3F”. Communication.
| HNO3 |
|
|
|
He |
| LiNO3 |
Be(NO3)2 |
B(NO
3)−
4 |
C |
NO−
3,
NH4NO3 |
O |
FNO3 |
Ne |
| NaNO3 |
Mg(NO3)2 |
Al(NO3)3 |
Si |
P |
S |
ClNO3 |
Ar |
| KNO3 |
Ca(NO3)2 |
Sc(NO3)3 |
Ti(NO3)4,
TiO(NO3)2 |
V(NO3)2,
V(NO3)3,
VO(NO3)2,
VO(NO3)3,
VO2NO3 |
Cr(NO3)2,
Cr(NO3)3,
CrO2(NO3)2 |
Mn(NO3)2,
Mn(NO3)3 |
Fe(NO3)2,
Fe(NO3)3 |
Co(NO3)2,
Co(NO3)3 |
Ni(NO3)2 |
CuNO3,
Cu(NO3)2 |
Zn(NO3)2 |
Ga(NO3)3 |
Ge |
As |
Se |
BrNO3 |
Kr |
| RbNO3 |
Sr(NO3)2 |
Y(NO3)3 |
Zr(NO3)4,
ZrO(NO3)2 |
Nb |
Mo(NO3)2,
Mo(NO3)3,
Mo(NO3)4,
Mo(NO3)6 |
Tc |
Ru(NO3)3 |
Rh(NO3)3 |
Pd(NO3)2,
Pd(NO3)4 |
AgNO3,
Ag(NO3)2 |
Cd(NO3)2 |
In(NO3)3 |
Sn(NO3)2,
Sn(NO3)4 |
Sb(NO3)3 |
Te |
INO3 |
Xe(NO3)2 |
| CsNO3 |
Ba(NO3)2 |
|
Hf(NO3)4,
HfO(NO3)2 |
Ta |
W(NO3)6 |
ReO3NO3 |
Os(NO3)2 |
Ir3O(NO3)10 |
Pt(NO3)2,
Pt(NO3)4 |
HAu(NO3)4 |
Hg2(NO3)2,
Hg(NO3)2 |
TlNO3,
Tl(NO3)3 |
Pb(NO3)2 |
Bi(NO3)3,
BiO(NO3) |
Po(NO3)2,
Po(NO3)4 |
At |
Rn |
| FrNO3 |
Ra(NO3)2 |
|
Rf |
Db |
Sg |
Bh |
Hs |
Mt |
Ds |
Rg |
Cn |
Nh |
Fl |
Mc |
Lv |
Ts |
Og |
|
↓ |
|
|
| La(NO3)3 |
Ce(NO3)3,
Ce(NO3)4 |
Pr(NO3)3 |
Nd(NO3)3 |
Pm(NO3)2,
Pm(NO3)3 |
Sm(NO3)3 |
Eu(NO3)3 |
Gd(NO3)3 |
Tb(NO3)3 |
Dy(NO3)3 |
Ho(NO3)3 |
Er(NO3)3 |
Tm(NO3)3 |
Yb(NO3)3 |
Lu(NO3)3 |
| Ac(NO3)3 |
Th(NO3)4 |
PaO(NO3)3 |
U(NO3)4,
UO2(NO3)2 |
Np(NO3)4 |
Pu(NO3)4,
PuO2(NO3)2 |
Am(NO3)3 |
Cm(NO3)3 |
Bk(NO3)3 |
Cf(NO3)3 |
Es |
Fm |
Md |
No |
Lr |

