氟磺酸
化合物 / 维基百科,自由的 encyclopedia
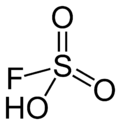
氟磺酸(化学式:HSO3F),或称氟代硫酸,是通用的强酸之一。其分子结构以HSO3F描述较恰当,可以强调它和硫酸(H2SO4)的关系。HSO3F是四面体型分子。
Quick Facts 氟磺酸, 识别 ...
| 氟磺酸 | |||
|---|---|---|---|
| |||

| |||
| IUPAC名 Sulfurofluoridic acid | |||
| 系统名 Fluorosulfuric acid[来源请求] | |||
| 别名 | 氟硫酸、氟代硫酸、 氟代磺酸 | ||
| 识别 | |||
| CAS号 | 7789-21-1 | ||
| PubChem | 24603 | ||
| ChemSpider | 23005 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | UQSQSQZYBQSBJZ-UHFFFAOYAW | ||
| UN编号 | 1777 | ||
| EINECS | 232-149-4 | ||
| RTECS | LP0715000 | ||
| MeSH | Fluorosulfonic+acid | ||
| 性质 | |||
| 化学式 | HFO3S | ||
| 摩尔质量 | 100.07 g·mol−1 | ||
| 外观 | 无色液体 | ||
| 密度 | 1.84 g cm-3 | ||
| 熔点 | -87 °C(185.7 K) | ||
| 沸点 | 165 °C(438.5 K) | ||
| 溶解性(水) | 可溶 | ||
| pKa | -10 | ||
| pKb | 24 | ||
| 结构 | |||
| 配位几何 | 四面体 | ||
| 分子构型 | 四面体 | ||
| 危险性 | |||
| 警示术语 | R:R20, R35 | ||
| 安全术语 | S:S1/2, S26, S45 | ||
| MSDS | ICSC 0996 | ||
| 欧盟编号 | 016-018-00-7 | ||
| 欧盟分类 | |||
| 相关物质 | |||
| 相关化学品 | 五氟化锑、三氟甲磺酸、 氢氟酸 | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
Close