热门问题
时间线
聊天
视角
三氟化溴
化合物 来自维基百科,自由的百科全书
Remove ads
三氟化溴是一種鹵素互化物,化學式為BrF3。這種無色、有毒、有腐蝕性的液體可溶於硫酸,但與水或有機化合物接觸會發生爆炸。它是一種強氟化劑和無機離子化溶劑。它在核燃料生產和後處理過程中被用於生產六氟化鈾(UF6)。[2]
Remove ads
製備
三氟化溴最早由保羅·利比奧(Paul Lebeau)於1906年報道。他將溴單質與氟在20 °C下反應得到了三氟化溴:[3]
Remove ads
結構
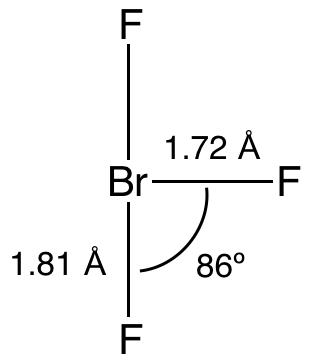
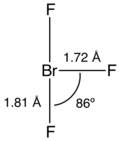
與ClF3和IF3類似,BrF3分子也是T形的。價層電子對互斥理論中,中心溴原子連有兩對孤對電子。每個軸向的Br-F鍵長度為1.81 Å,而水平方向的為1.72 Å。軸向Br-F鍵與水平Br-F鍵的夾角略小於90°,86.2°的鍵角是因為孤對電子的排斥比成鍵電子更強,鍵角的變小使得能量降低。[5][6]
化學性質
BrF3是一種強氟化劑,但略弱於ClF3。這種液體能導電,因為它能發生自耦電離:[2]
許多離子型氟化物易溶於三氟化溴,並形成溶劑合鹼(即路易斯酸鹼的加合物):[2]
此外少數共價型氟化物,例如四氟化矽、五氟化釩及類似化合物也可溶於三氟化溴,它們在溶液中作為路易斯酸。
含BrF2+的物質與含BrF4-能發生類似於酸鹼中和的反應:
這類反應被廣泛用於製取含氟配合物,例如AgAuF4、(NO2)SnF6、(NO)2SnF6、LiVF6、KRuF6等,在上述反應完成後真空蒸發除去三氟化溴即可得到產品。
三氟化溴能使高價氟配合物穩定,例如四氟化鈀不能分離得到,但在三氟化溴中可製得它的配合物。稀有氣體的氟化物也能在三氟化溴中與強路易斯酸形成加合物。[7]
Remove ads
參考資料
外部連結
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads