热门问题
时间线
聊天
视角
視紫質
来自维基百科,自由的百科全书
Remove ads
視紫質[1](英語:rhodopsin)也稱視紫紅質、視紫蛋白[2]、視紫素[3]、視網膜紫質[4][5],是大多數脊椎動物視網膜視桿細胞中亮紫紅色的光敏視色素,其由視蛋白和11-順視黃醛輔基結合而成,最大光吸收在500nm附近,可將所吸收的光信號轉化為跨膜電信號,其光電響應是視覺形成的最初階段。
視紫質是一種由RHO基因編碼的蛋白質[6],屬於G蛋白偶聯受體(GPCR)的一種。當視紫質暴露在光線下時,會迅速發生光漂白。在人體中,它會在大約30分鐘內完全還原,之後,視杆就會變得更加敏感[7]。RHO 基因發生缺陷會導致多種眼科疾病,例如色素性視網膜炎和先天性停滯性夜盲症。
Remove ads
歷史
視紫質最早是由德國生理學家Franz Christian Boll在1876年發現的。術語 rhodopsin 源自古希臘語 ῥόδον(rhódon,rose)「玫瑰色」之義,與 ὄψις(ópsis,sight)「視覺、視力」之義。[8] 這個名稱由德國生理學家威廉·屈內 (德語:Wilhelm Friedrich Kühne, 1837-1900年)於1878年提出。[9][10]
喬治·沃爾德(George Wald)發現視紫質是一種全蛋白(holoprotein),由視黃醛和載脂蛋白(apoprotein)組成,他將其命名為視蛋白(opsin),而今天它被更狹義地描述為apo-rhodopsin。[11] 如今,「opsin」 一詞被更廣泛地用於指一類與視黃醛結合、因而成為對光敏感的 G 蛋白偶聯受體(光感受蛋白),包括所有與之密切相關的蛋白質。[12][13][14] 當沃爾德及其同事後來從雞視網膜中分離出碘視紫質(iodopsin),從而發現了首個已知的視錐視蛋白(cone opsin)時,他們將其對應的載脂蛋白(apo-iodopsin)稱為 photopsin(意指其參與明視覺,photopic vision),而將 apo-rhodopsin 稱為 scotopsin(意指其參與暗視覺,scotopic vision)。[15]
視紫質基因突變會影響視力,比如夜盲症等。
微生物也有視紫質,但沒有和G蛋白耦合,因此不屬於G蛋白偶聯受體。儘管如此,原核生物視紫質仍然被看作是和GPCR同屬一超科。
Remove ads
概述
視紫質是一種存在於視杆細胞外段盤狀結構中的蛋白質。它介導的是暗視覺(scotopic vision),也就是在微弱光照條件下的單色視覺。[7][16] 視紫質對藍綠光(約 500 nm)的吸收最強,[17][18] 因此在反射光下呈現出略帶紅紫色的外觀,這也是它早期被稱為「視覺紫質(visual purple)」的原因。
有若干與視紫質密切相關的視蛋白(opsin),它們之間只在少數胺基酸殘基上有所不同,並且在最強吸收的光波長上也略有差異。包括視紫質在內,人類共有 9 種視蛋白,[12] 另外還有一種名為隱花色素(cryptochrome)的光敏蛋白(對光敏感,但不屬於 opsin 家族)。[19]
結構

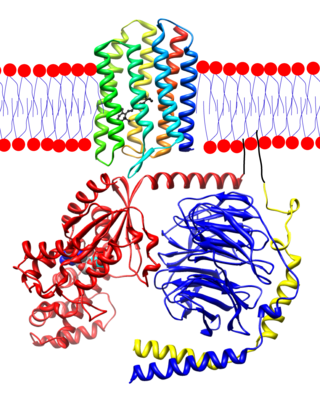
視紫質與其他視蛋白類似,屬於一類 G 蛋白偶聯受體(G-protein-coupled receptor, GPCR)。[20][21] GPCR 是一類化學感受器(chemoreceptors),嵌入在細胞膜的脂質雙層中,具有七個跨膜結構域,這些結構域共同構成一個可與配體結合的口袋。[22][23] 對於視紫質而言,其配體是 來源於維生素A的發色團11-順-視黃醛(11-cis-retinal),[24][25][26][27][28] 它以近乎平行的方式嵌入細胞膜[29],並通過席夫鹼(Schiff base)鍵與第七個跨膜結構域中的一個賴氨酸殘基(Lys296)共價結合。[30][31][32][33] 然而,11-順-視黃醛本身只是堵住了受體的結合口袋,並不會激活視紫質。只有當 11-順-視黃醛吸收光子並發生構型改變,異構化為全反式視黃醛(all-trans-retinal)時,[34][35] 受體才進入激活構型,[36][37] 引起視紫質整體構象變化,[36] 從而啟動下游的光傳導級聯反應(phototransduction cascade)。[38] 也就是說,一個原本作為化學感受器的受體,在此過程中被「轉化」為對光敏感的光感受器。[13]
與視黃醛結合的那一個賴氨酸殘基在幾乎所有視蛋白中都是高度保守的,只有極少數視蛋白在進化過程中失去了這一殘基。[13] 缺少該賴氨酸位點的視蛋白(包括視紫質在相應突變下)將不再對光敏感。[39][40][41] 其中一些突變會使視紫質在沒有光照的情況下也處於構成性(持續)活化狀態。[42][43][44] 即使是野生型視紫質,在不結合11-順-視黃醛時也會表現出一定程度的構成性活性,只是弱得多。[45] 因此,11-順-視黃醛在功能上可以被視為一種反向激動劑(inverse agonist)。此類突變是常染色體顯性視網膜色素變性(autosomal dominant retinitis pigmentosa) 的病因之一。[44] 在人工條件下,可以將與視黃醛結合的賴氨酸殘基移動到蛋白質中的其他位置,甚至移動到其他跨膜結構域中,而並不會改變視紫質的活性。[46]
牛的視紫質由348個胺基酸組成,其中與視黃醛結合的賴氨酸為Lys296。它是首個被完全解析胺基酸序列[47] 和三維結構的視蛋白,其結構已通過對視紫質晶體進行X射線晶體學分析而得到深入研究。[48] 為了解釋視黃醛基團如何在不與包圍它的蛋白口袋發生嚴重空間衝突的情況下改變構象,人們提出了多個模型,例如 「雙輪-腳踏車(bicycle-pedal)機制」、「呼啦圈扭轉(hula-twist)機制」 等。[49][50][51] 最近的數據支持這樣一種觀點:視紫質在功能上主要以單體(monomer)形式存在,而不是長期以來GPCR研究中所認為的二聚體形式。[52]
在其天然所在的膜環境中,視紫質以高密度排列,這有利於其捕獲光子,因為在膜中高度堆積時,單個光子更有機會被某個視紫質分子吸收。然而,這種高密度在G蛋白信號傳導方面也帶來劣勢:由於膜中過於擁擠、充滿視紫質,信號傳遞所需的G蛋白及其他分子的擴散變得更加困難,從而對信號級聯造成一定限制。[53]
光信號轉導
視紫質是光信號轉導中必不可少的一種G蛋白偶聯受體。

在視紫質分子中,視黃醛(retinal)的醛基通過一個質子化的席夫鹼鍵(-NH⁺=CH-)與蛋白質上一處賴氨酸殘基的氨基共價連接在一起。[30] 當視紫質吸收光子後,其視黃醛輔因子會從11-順構型(11-cis)異構化為全反式構型(all-trans),隨後蛋白質本身經歷一系列構象鬆弛,以適應該已異構化輔因子的形狀變化。在這一過程中形成的若干中間態,最早在喬治·沃爾德(George Wald)的實驗室中得到研究,他也因這方面的工作於 1967 年獲得了諾貝爾獎。[54]
之後,研究者藉助時間分辨紅外光譜(time-resolved IR spectroscopy)和紫外/可見光譜(UV/Vis spectroscopy)進一步研究了這一光異構化的動力學過程。第一個光產物 photorhodopsin 會在照射後約 200 飛秒內形成,隨後在皮秒尺度內生成第二個產物 bathorhodopsin,其中的全反式鍵處於扭曲狀態。該中間態可以在低溫冷凍條件下被「捕獲」並加以研究,最初曾被稱為 prelumirhodopsin。[55] 在隨後出現的中間態 lumirhodopsin 和 metarhodopsin I 中,與全反式視黃醛相連的席夫鹼鍵仍然保持質子化,蛋白整體保持紅色外觀。真正引發神經興奮的關鍵變化,是 metarhodopsin I 向 metarhodopsin II 的轉變,伴隨著席夫鹼鍵的去質子化以及顏色由紅色變為黃色。[56]
Remove ads
參見主條目:視覺光信號轉導(Visual phototransduction)
光激活的產物 metarhodopsin II(Meta II) 通過激活G蛋白 transducin(Gt) 啟動視覺光信號轉導的第二信使通路,並導致其α亞基從複合體中被釋放出來。這個結合了三磷酸鳥苷(GTP)的α亞基進一步激活 cGMP磷酸二酯酶。該酶會水解(降解)cGMP,從而降低其局部濃度,使其不再足以激活cGMP依賴的陽離子通道。通道關閉導致感光細胞膜發生超極化(hyperpolarization),進而改變它們釋放神經遞質的速率。[57][38]
Meta II(metarhodopsin II)在激活 transducin 之後,會被視紫質激酶(rhodopsin kinase)和arrestin(阻遏蛋白)迅速失活。[58] 為了使後續的光信號轉導得以繼續進行,視紫質色素必須再生,這意味著需要將全反式視黃醛重新被替換為11-順視黃醛,而 Meta II 的衰變在這一過程中至關重要。
在 Meta II 衰變的過程中,將全反式視黃醛與載體蛋白視蛋白(opsin,亦稱 aporhodopsin)連接在一起的席夫鹼鍵被水解,並形成中間態 Meta III。在桿狀細胞外段中,Meta III 進一步衰變為游離的全反式視黃醛和視蛋白。[58] Meta II 衰變的另一種產物是全反式視黃醛–視蛋白複合物,其中全反式視黃醛被轉移到了第二個結合位點上。Meta II 的衰變是走向 Meta III,還是形成全反式視黃醛–視蛋白複合物,似乎取決於反應環境的 pH 值:較高的 pH 傾向於推動反應朝 Meta III 方向進行。[58]
Remove ads
視網膜疾病
視紫質基因的突變在多種視網膜疾病中起重要作用,例如 色素性視網膜炎(retinitis pigmentosa)。一般而言,缺陷視紫質會與泛素(ubiquitin)在包涵體(inclusion bodies)中聚集,破壞中間絲(中間纖維)網絡,並削弱細胞降解失功能蛋白的能力,最終導致感光細胞發生凋亡(apoptosis)。[59]
另一些發生在視紫質上的突變則導致 X 連鎖先天性停滯性夜盲,其主要機制是由於視紫質的構成性(持續)激活,特別是當突變位於與發色團結合口袋周圍時。[60] 此外,研究還發現了多種與視紫質相關的病理狀態,包括:高爾基體後運輸(post-Golgi trafficking)不良、異常的受體激活、桿狀細胞外段的不穩定,以及異常的 arrestin 結合等。[60]
參見
- 細菌視紫質(bacteriorhodopsin)——一種存在於某些嗜鹽古菌中的蛋白質,作為光碟機動的質子泵。
參考文獻
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads