
Ácido etanoico
De Wikipedia, a enciclopédia encyclopedia
O ácido acético (do latim acetum, azedo), CH3COOH, oficialmente chamado ácido etanoico, é um ácido carboxílico (especificamente, um ácido monocarboxílico), saturado e de cadeia aberta. Em sua forma impura, é popularmente conhecido como vinagre (±4.0% de ácido acético em solução aquosa). Quando está livre de água é conhecido como ácido acético glacial. É conhecido por ser um ácido fraco, corrosivo, com vapores que causam irritação nos olhos, ardor no nariz e garganta e congestão pulmonar. Um reagente químico importante e largamente utilizado na indústria química, usado na produção de politereftalato de etileno (PET), sendo este utilizado em garrafas de bebidas, o acetato de celulose utilizado na película fotográfica, o acetato de polivinil utilizado na cola de madeira, também utilizado para limpeza e desinfecção. A demanda global do ácido acético é em torno de 6,5 milhão toneladas por ano, desta aproximadamente 1,5 Mt/a são encontrados a partir da reciclagem; o restante é manufaturado dos estoques petroquímicos ou das fontes biológicas.
| Ácido etanoico Alerta sobre risco à saúde | |
|---|---|
 |
 |
 |
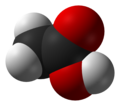 |
| Nome IUPAC | Ácido etanóico |
| Nome sistemático | Ácido Acético |
| Outros nomes | Hidróxido de acetil (AcOH), Acetato de hidrogênio (HAc), ácido acético, Ácido metanocarboxílico |
| Identificadores | |
| Número CAS | 64-19-7 |
| PubChem | 176 |
| ChemSpider | 171 |
| SMILES |
|
| InChI | 1/C2H4O2/c1-2(3)4/h1H3,(H,3,4) |
| Propriedades | |
| Fórmula química | C2H4O2 |
| Massa molar | 60.04 g mol-1 |
| Aparência | líquido incolor |
| Densidade | 1.049 g/cm3 (l) 1.266 g/cm3 (s) |
| Ponto de fusão |
16.5 °C, 290 K, 62 °F |
| Ponto de ebulição |
118.1 °C, 391 K, 245 °F |
| Solubilidade em água | completamente miscível |
| Acidez (pKa) | 4,75 a 25 °C |
| Viscosidade | 1.22 mPa·s a 25 °C |
| Estrutura | |
| Momento dipolar | 1.74 D (gas) |
| Riscos associados | |
| Classificação UE | |
| NFPA 704 | |
| Frases R | R10, R35 |
| Frases S | S1/2, S23, S26, S45 |
| Ponto de fulgor | 43 °C |
| LD50 | 3310 mg/kg, oral (ratos) |
| Compostos relacionados | |
| Outros aniões/ânions | Acetamida Cloreto de acetila Ácido tioacético |
| Ácidos carboxílicos relacionados | Ácido fórmico (C1:0) Ácido oxálico (etanodioico) Ácido glicólico (hidroxietanoico) Ácido propiônico (C3:0) |
| Compostos relacionados | Acetato de metila Anidrido acético Acetaldeído Etanol Acetato de sódio |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
O ácido acético é obtido industrialmente através de variadas tecnologias e matérias primas. Com relação à matéria prima, de origem fóssil pode-se citar o petróleo e carvão, e de fontes renováveis, a cana de açúcar. Os processos a partir de fontes fósseis são os mais utilizados para a obtenção do produto e destaca-se a carbonilação de metanol, que é responsável pela maior parte do ácido acético produzido em escala mundial.
O ácido acético é uma molécula central na bioquímica, e é produzido em alguma proporção por quase todas as formas de vida.
