Табун (хімічная зброя)
хімічнае злучэнне From Wikipedia, the free encyclopedia
Remove ads
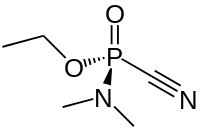
Табу́н[1] (этылавы эфір дыметыламіда цыянафосфарнай кіслаты) — фосфарарганічнае злучэнне. Атрутнае рэчыва нервова-паралітычнага дзеяння. Выклікае моцны міёз.


Бясколерная рухомая вадкасць тэмпература кіпення 220 (240[2][1], каля 230[3]) °C, тэмпература плаўлення −50[1][3] (−48[2]) °C. Шчыльнасць 1077,8 кг/м³[1] (1087 г/см³[3]). Дрэнна раствараецца ў вадзе (каля 12 %), добра ў арганічных растваральніках.
Remove ads
Сінтэз і ўласцівасці
Табун атрымоўваюць паслядоўным узаемадзеяннем хлорвокісу фосфара POCl3 са злішкам дыметыламіна, потым з этанолам і цыянідам калію:
- POCl3 + 2(CH3)2NH (CH3)2NP(O)Cl2 + (CH3)2NH•HCl
- (CH3)2NP(O)Cl2 + C2H5OH (CH3)2NP(O)ClOC2H5 + HCl
- (CH3)2NP(O)ClOC2H5 + KCN (CH3)2NP(O)(CN)OC2H5 + KCl
Упершыню атрымаў нямецкі хімік Герхард Шрадэр.
Павольна гідралізуецца вадой, у кіслым асяроддзі гідроліз паскараецца, пры гэтым адбываецца адўчапленне дыэтыламіднай групы:
- (CH3)2NP(O)(CN)OC2H5 + H2O + HCl (CH3)2NH•HCl + HOP(O)(CN)OC2H5
Хутка гідралізуецца ў растворах шчолачаў, адшчапляе цыянід-іён:
- (CH3)2NP(O)(CN)OC2H5 + NaOH (CH3)2NP(O)(OH)OC2H5 + NaCN
Лёгка ўзаемадзейнічае з растворамі аміяку і амінаў, што выкарыстоўваецца для дэгазацыі табуна. Прадукты дэгазацыі з’яўляюцца ядавітымі, бо ўтрымоўваюць солі сінільнай кіслаты.
Remove ads
Гл. таксама
- Зарын
- VX
- GV
Зноскі
Літаратура
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads