From Wikipedia, the free encyclopedia
Egzozomski kompleks (ili PM/Scl kompleks, koji se često naziva egzozom) je multiproteinski unutarćelijski kompleks, sposoban da razgradi različite vrste molekula RNK (ribonukleinske kiseline). Kompleksi egzosoma nalaze se u eukariotskim ćelijama i kod archaea, dok u bakterijama obavlja jednostavniji kompleks slične funkcije zvani degradosom.

Jezgro egzosoma sadrži šesteročlanu prstenastu strukturu za koju su vezani drugi proteini. U eukariotskim ćelijama, egzosomski kompleks je prisutan u citoplazmi, jedru, a posebno jedarcetu, iako različiti proteini stupaju u interakciju sa kompleksom egzosoma u ovim odjeljcima, regulišući degradacijsku RNK aktivnost kompleksa na supstrate specifične za ove ćelijske odjeljke. Supstrati egzosoma uključuju informacijsku RNK, rRNK i mnoge tipove malih RNK. Egzozom ima egzoribonukleolitsku funkciju, što znači da razgrađuje RNK počevši od jednog kraja (3′ kraj u ovom slučaju), a kod eukariota i endoribonukleolitsku funkciju, što znači da cijepa RNK na mjestima unutar molekula.
Nekoliko proteina u egzosomu su meta autoantitijela kod pacijenata sa specifičnim autoimuniskm bolestima (posebno PM/Scl sindrom preklapanja) i nekim antimetaboličkim hemoterapijama za funkciju raka, blokiranjem aktivnosti egzosoma. Pored toga, mutacije u ekzozomskoj komponentI 3 uzrokuju pontocerebelumsku hipoplaziju i spinalnu bolest motornih neurona.
Egzozom je prvi put otkriven kao RNaza 1997. godine u pupajućim kvascima Saccharomyces cerevisiae, često korišćenom modelnom organizmu.[1] Nedugo zatim, 1999., shvatilo se da je egzosom zapravo ekvivalent kvasca već opisanog kompleksa u ljudskim ćelijama zvanog PM/Scl kompleks, koji je identificiran kao autoantigen kod pacijenata sa određenim autoimunskim bolestima godinama ranije (vidi ispod).[2] Prečišćavanje ovog "PM/Scl kompleksa" omogućilo je identifikaciju više ljudskih egzosomskih proteina i na kraju karakterizaciju svih komponenti u kompleksu.[3][4] U 2001., sve veća količina podataka o genomu, koja je postala dostupna, omogućila je predviđanje egzosomskih proteina u arhejama, iako će trebati još dvije godine prije nego što prvi egzosomski kompleks iz arhejskog organizma bude prečišćen.[5][6]

Jezgro kompleksa ima prstenastu strukturu koja se sastoji od šest proteina koji svi pripadaju istoj klasi Rnaza, proteina sličnih RNaza PH.[7] U arhejama postoje dva različita proteina slična PH (zvana Rrp41 i Rrp42), svaki prisutan po tri puta naizmjeničnim redoslijedom. Eukariotski egzosomski kompleksi imaju šest različitih proteina koji formiraju prstenastu strukturu.[8][9] Od ovih šest eukariotskih proteina, tri liče na arhejski protein Rrp41, a ostala tri proteina su sličnija arhejskom proteinu Rrp42.[10]

Na vrhu ovog prstena nalaze se tri proteina koji imaju S1 RNK-vezujući domen (RBD). Dva proteina pored toga imaju K-homologni (KH) domen.[7] Kod eukariota, tri različita "S1" proteina su vezana za prsten, dok kod arheja bilo jedan ili dva različita "S1" proteina mogu biti dio egzosoma (iako uvijek postoje tri S1 podjedinice vezane za kompleks).[11]
Ova prstenasta struktura je vrlo slična onoj kod proteina RNaza PH i PNPaza. U bakterijama, protein RNaza PH, koji je uključen u procesuiranje tRNK, formira heksamerni prsten koji se sastoji od šest identičnih RNK PH proteina.[12][13] U slučaju PNPaze, koja je fosforolitski protein koji razgrađuje RNK koji se nalazi u bakterijama, hloroplastima i mitohondrijama nekih eukariotskih organizama, dvije Rnaze PH domena, i oba S1 i KH RNK-vezujuća domena dio je jednog proteina, koji formira trimerni kompleks koji usvaja strukturu gotovo identičnu onoj kod egzosoma.[14] Zbog ove velike sličnosti u domenima i strukturi proteina, smatra se da su ovi kompleksi evolucijski skoro povezani i da imaju zajedničkog pretka.[15] Proteini egzosoma slični RNazi PH, PNPaza i RNaza PH svi pripadaju porodici Rnaza PH RNaza i fosforolitske su egzoribonukleaze, što znači da koriste anorganski fosfat za uklanjanje nukleotida iz 3' kraja molekula RNK.[7]
Osim ovih devet jezgarnih egzosomskih proteina, dva druga proteina se često povezuju s kompleksom u eukariotskim organizmima. Jedan od njih je Rrp44, hidrolitska RNKaza, koja pripada porodici RNaza R, hidrolitskih eksoribonukleaza (nukleaze koje koriste vodu za cijepanje nukleotidne veze). Osim što je egzoribonukleolitski enzim, Rrp44 ima i endoribonukleolitsku aktivnost, koja se nalazi u zasebnom domenu proteina.[16][17] U kvascima, Rrp44 je povezan sa svim kompleksima egzosoma i ima ključnu ulogu u aktivnosti egzosomskog kompleksa kvasca.[18] Iako ljudski homolog proteina postoji, dugo vremena nisu pronađeni dokazi da je njegov ljudski homolog povezan s ljudskim egzosomskim kompleksom.[7] Međutim, 2010. otkriveno je da ljudi imaju tri Rrp44 homologa i dva od njih mogu biti povezani sa kompleksom egzosoma. Ova dva proteina najvjerovatnije razgrađuju različite supstrate RNK zbog njihove različite ćelijske lokalizacije, pri čemu je jedan lokaliziran u citoplazmi (DIS3L1), a drugi u jedru (DIS3).[19][20]

Druga uobičajena vezana boja. protein se naziva Rrp6 (kod kvasca) ili PM/Scl-100 (kod ljudi). Kao i Rrp44, ovaj protein je hidrolitska egzoribonukleaza, ali u ovom slučaju iz porodice proteina RNaza D.[21] Protein PM/Scl-100 je najčešće dio kompleksa egzosoma u ćelijskim jedrima, ali može činiti i dio citoplazmatskog egzosomskog kompleksa.[22]
Osim ove dvije čvrsto vezane proteinske podjedinice, mnogi proteini stupaju u interakciju s kompleksom egzosoma iu citoplazmi i u ćelijskom jedru. Ovi slabo povezani proteini mogu regulisati aktivnost i specifičnost kompleksa egzosoma. U citoplazmi, egzosom stupa u interakciju sa AU bogatim elementom (ARE) vezujućim proteinima (npr. KRSP i TTP), koji mogu promovirati ili spriječiti degradaciju iRNK. Jedarni egzosom se povezuje s proteinima koji vežu RNK (npr. MPP6/Mpp6 i C1D/Rrp47 kod ljudi/kvasca) koji su potrebni za obradu određenih supstrata.[7]
Osim pojedinačnih proteina, ostali proteinski kompleksi stupaju u interakciju s egzosomom. Jedan od njih je citoplazmatski Ski-kompleks, koji uključuje RNK-helikazu (Ski2) i uključen je u degradaciju iRNK.[23] U jedru, procesuiranje rRNK i snoRNK od posreduje egzosomni TRAMP-kompleks, koji sadrži i RNK-helikazu (Mtr4) i poliadenilacijsku aktivnost (Trf4).[24]
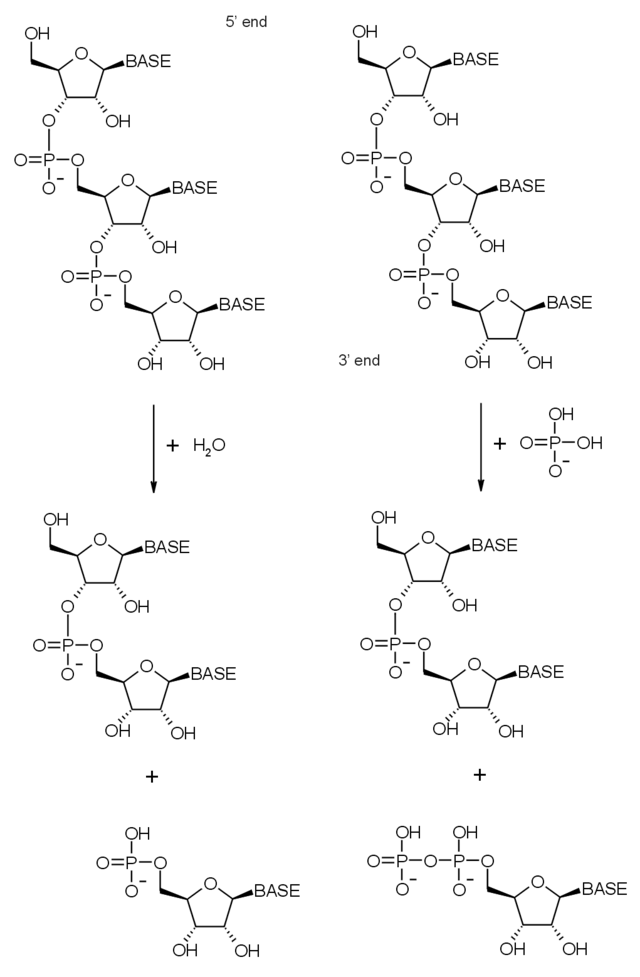
Kao što je gore navedeno, egzosomni kompleks sadrži mnogo proteina sa domenima ribonukleaze. Tačna priroda ovih domena ribonukleaze mijenjala se kroz evoluciju, od bakterijskih preko arhejskih do eukariotskih kompleksa kako su se dobivale i gubile različite aktivnosti. Egzozom je prvenstveno 3'-5' egzoribonukleaza, što znači da razgrađuje molekule RNK sa njihovog 3' kraja. Egzoribonukleaze sadržane u egzosomnim kompleksima su ili fosforolitske (proteini slični RNazi PH) ili, kod eukariota, hidrolitske (proteini domena RNaza R i Rnaza D). Fosforolitski enzimi koriste anorganski fosfat za cijepanje fosfodiesterske veze – oslobađajući nukleotid-difosfate. Hidrolitski enzimi koriste vodu da hidroliziraju ove veze – oslobađajući nukleotid monofosfate.
Kod arheja, Rrp41 podjedinica kompleksa je fosforolitska egzoribonukleaza. Tri kopije ovog proteina prisutne su u prstenu i odgovorne su za aktivnost kompleksa.[9] Kod eukariota, nijedna od podjedinica RNaza PH nije zadržala ovu katalitsku aktivnost, što znači strukturu jezgra prstena ljudski egzosom nema enzimski aktivan protein.[25] Unatoč ovom gubitku katalitske aktivnosti, struktura egzosomnog jezgra je visoko konzervirana od arheja do ljudi, što sugeriše da kompleks obavlja vitalnu ćelijsku funkciju. Kod eukariota, odsustvo fosforolitske aktivnosti nadoknađuje se prisustvom hidrolitskih enzima, koji su odgovorni za ribonukleaznu aktivnost egzosoma u takvim organizmima.<.[26][27][28]
Kao što je gore navedeno, hidrolitski proteini Rrp6 i Rrp44 povezani su sa egzosomom kod kvasca i kod ljudi, osim Rrp6, dva različita proteina, Dis3 i Dis3L1, mogu biti povezana na poziciji Rrp44 proteina kvasaca.[19][20] Iako se prvobitno smatralo da proteini domena S1 imaju i 3'-5' hidrolitsku egzoribonukleaznu aktivnost, postojanje ove aktivnosti je nedavno dovedeno u pitanje i ovi proteini bi mogli imati samo ulogu u vezujući supstrati prije njihove degradacije kompleksom.[26]

Egzozom je uključen u degradaciju i obradu širokog spektra tipova RNK. U citoplazmi ćelija, on je uključen u preokret molekula informacijske RNK (iRNK). Kompleks može razgraditi molekule iRNK koje su označene za degradaciju jer sadrže greške, kroz interakcije s proteinima iz nonsens posredovanog razlaganja ili neprekidnog razlaganja puteva. Na alternativni način, iRNK se razgrađuju kao dio njihovog normalnog prometa. Nekoliko proteina koji stabiliziraju ili destabiliziraju molekule iRNK, vezivanjem za elemente bogate AU u 3' neprevedenoj regiji iRNK, u interakciji sa egzosomskim kompleksom.[29][30][31] U jedru, egzosom je potreban za ispravnu obradu nekoliko molekula male jedarne RNK.[32] Konačno, jedarce je odjeljak u kojem se nalazi većina egzosomskog kompleksa. Tamo ima ulogu u procesuiranju 5.8S ribosomske RNK (prva identifikovana funkcija egzosoma) i nekoliko malih nukleolusnih RNK.[1][32][33]
Iako većina ćelija ima druge enzime koji mogu razgraditi RNK, bilo sa 3' ili sa 5' kraja RNK, egzosomski kompleks je neophodan za opstanak ćelije. Kada se ekspresija egzosomskih proteina umjetno smanji ili zaustavi, naprimjer RNK-interferencija, rast se zaustavlja i ćelije na kraju umiru. Oba glavna proteina egzosomskog kompleksa, kao i dva glavna povezana proteina, su esencijalni proteini.[34] Bacteria nemaju egzosomski kompleks; međutim, slične funkcije obavlja jednostavniji kompleks koji uključuje protein PNPaza, nazvan degradosom.[35]

Egzosom je ključni kompleks u kontroli kvaliteta ćelijske RNK. Za razliku od prokariota, eukarioti posjeduju visoko aktivne sisteme za nadzor RNK koji prepoznaju neprerađene i pogrešno obrađene komplekse RNK-protein (kao što su ribosomi) prije njihovog izlaska iz jedra. Pretpostavlja se da ovaj sistem sprečava aberantne komplekse da ometaju važne ćelijske procese kao što je sinteza proteina.[36]
Pored prerade RNK, prometa i aktivnosti nadzora, egzosom je važan za degradaciju takozvanih kriptično nestabilnih transkripta (CUT-ova) koji se proizvode iz hiljada lokusa unutar genoma kvasca.[37][38] Važnost ovih nestabilnih RNK i njihova degradacija su još uvijek nejasni, ali slični tipovi RNK su također otkriveni i u ljudskim ćelijama.[39]
Egzosomski kompleks je meta autoantitijela kod pacijenata s različitim autoimunskim bolestima. Ova autoantitijela se uglavnom nalaze kod ljudi sa PM/Scl sindromom preklapanja, autoimunskom bolešću u kojoj pacijenti imaju simptome i skleroderma i polimiozitisa ili dermatomiozitisa.[40] Autoantitijela se mogu otkriti u serumu krvne plazme pacijenata raznim testovima. U prošlosti, najčešće korišteni metodi bili su dvostruka imunodifuzija korišćenjem ekstrakta telećih timusa, imunofluorescencijama na ćelijama HEp-2 ili imunoprecipitacijama iz ekstrakata ljudskih ćelija. U testovima imunoprecipitacije sa serumima iz antiegzosom pozitivnih seruma, precipitira se poseban skup proteina. Već godinama prije nego što je egzosomski kompleks identificiran, ovaj obrazac je nazvan PM/Scl kompleks.[41] Imunofluorescencija pomoću seruma ovih pacijenata obično pokazuje tipično bojenje ćelijskog jedarceta, što je izazvalo sugestiju da bi antigen prepoznat autoantitijelima mogao biti važan u sintezi ribosoma.[42] U skorije vrijeme, rekombinantni egzosomski proteini postali su dostupni i oni su korišteni za razvoj linijskih imunotestova (LIA) i enzimski vezan imunosorbentni test (ELISA) za otkrivanje ovih antitijela.[7]
Kod ovih bolesti, antitijela su uglavnom usmjerena na dva proteina kompleksa, zvana PM/Scl-100 (protein sličan RNazi D) i PM/Scl-75 (jedan od RNaza PH poput proteina iz prstena) i antitijela koja prepoznaju ove proteine nalaze se u otprilike 30% pacijenata sa sindromom preklapanja PM/Scl.[43] Iako su ova dva proteina glavna meta autoantitijela, druge podjedinice egzosoma i povezani proteini (poput C1D) mogu biti ciljani kod ovih pacijenata.[44][45] Danas, najosetljiviji način otkrivanja ovih antitiela je korišćenje peptida, dobijenog od PM/Scl-100 proteina, kao antigena u testu ELISA, umjesto kompletnih proteina. Ovom metodom, autoantitijela se nalaze kod do 55% pacijenata sa sindromom preklapanja PM/Scl, ali se mogu otkriti i kod pacijenata sa sklerodermom, polimiozitisom ili samo dermatomiozitisom.[46]
Kako se autoantitijela nalaze uglavnom kod pacijenata koji imaju karakteristike nekoliko različitih autoimunskih bolesti, klinički simptomi kod ovih pacijenata mogu uveliko varirati. Simptomi koji se najčešće viđaju su tipski simptomi pojedinačnih autoimunskih bolesti i uključuju Raynaudov fenomen, artritis, miozitis i sklerodermu.[47] Liječenje ovih pacijenata je simptosko i slično je liječenju individualne autoimunske bolesti, često uključuje ili imunosupresivne ili imunomodulatorne lijekove.[48]
Pokazalo se da egzosom inhibira antimetabolit fluorouracil, lijek koji se koristi u hemoterapijama karcinoma. To je jedan od najuspješnijih lijekova za liječenje čvrstih tumor a. U ćelijama kvasca tretiranim fluorouracilom, pronađeni su defekti u obradi ribosomske RNK identični onima uočenim kada je aktivnost egzosoma blokirana molekularskim biološkim strategijama. Nedostatak ispravne obrade ribosomske RNK je smrtonosan za ćelije, objašnjavajući antimetabolički učinak lijeka.[49]
Mutacije u komponenti egzosoma 3 uzrokuju infantilnu spinalnu bolest motornih neurona, cerebelarnu atrofiju, progresivnu mikrocefaliju i duboko globalno kašnjenje u razvoju, u skladu sa pontocerebelarnom hipoplazijom tipa 1B (.org/entry/614678 PCH1B; MIM 614678[mrtav link]).[50]
| Legenda | Opće ime | Domeni | Čovjek | Kvasac (S. cerevisiae) | Archaea | MW (kD) | Ljudski gen | Kvaščev gen |
|---|---|---|---|---|---|---|---|---|
| 1 | Csl4 | S1 RBD | hCsl4 | Csl4p/Ski4p | Csl4 | 21–32 | EXOSC1 | Šablon:Kvsščev gen |
| 2 | Rrp4 | S1/KH RBD | hRrp4 | Rrp4p | Rrp4 | 28–39 | EXOSC2 | Šablon:Kvaščev gen |
| 3 | Rrp40 | S1/KH RBD | hRrp40 | Rrp40p | (Rrp4)A | 27–32 | EXOSC3 | Šablon:Kvaščev gen |
| 4 | Rrp41 | RNaza PH | hRrp41 | Rrp41p/Ski6p | Rrp41C | 26–28 | EXOSC4 | Šablon:Kvaščev gen |
| 5 | Rrp46 | RNaza PH | hRrp46 | Rrp46p | (Rrp41)A,C | 25–28 | EXOSC5 | Šablon:Kvaščev gen |
| 6 | Mtr3 | RNaza PH | hMtr3 | Mtr3p | (Rrp41)A,C | 24–37 | EXOSC6 | Šablon:Yeast Gene |
| 7 | Rrp42 | RNaza PH | hRrp42 | Rrp42p | Rrp42 | 29–32 | EXOSC7 | Šablon:Kvaščev gen |
| 8 | Rrp43 | RNaza PH | OIP2 | Rrp43p | (Rrp42)A | 30–44 | EXOSC8 | Šablon:Kvaščev gen |
| 9 | Rrp45 | Rnaza PH | PM/Scl-75 | Rrp45p | (Rrp42)A | 34–49 | EXOSC9 | Šablon:Kvaščev gen |
| 10 | Rrp6 | RNaza D | PM/Scl-100C | Rrp6pC | n/a | 84–100 | EXOSC10 | Šablon:Kvaščev gen |
| 11 | Rrp44 | RNaza R | Dis3B,C | Rrp44p/Dis3pC | n/a | 105–113 | DIS3
DIS3L1 |
Šablon:Kvaščev gen |
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.