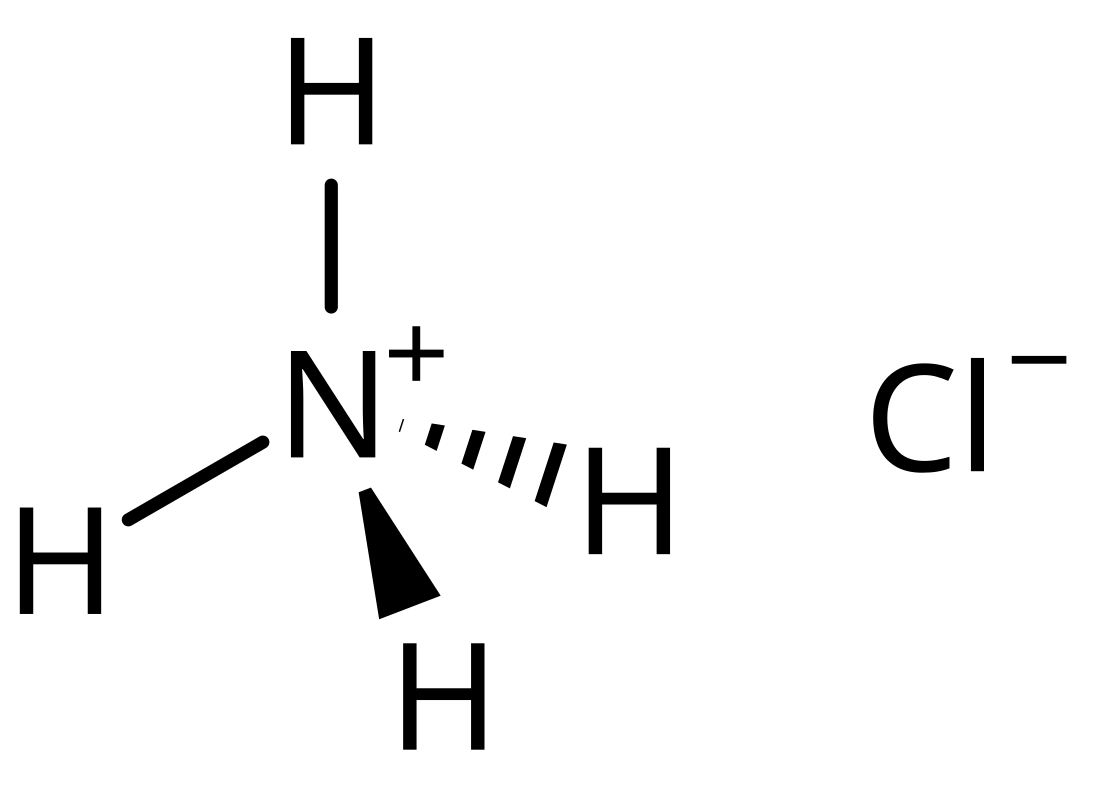
Amonij-hlorid
From Wikipedia, the free encyclopedia
Remove ads
Amonij-hlorid je neorganski spoj sa formulom NH4Cl. To je bijela kristalna so, vrlo dobro rastvorljiva u vodi. Rastvori amonij-hlorida su blago kiseli. "So amonijaka" (sal ammoniac ili salmijak) ime je prirodnog, mineraloškog oblika amonij-hlorida. Ovaj mineral obično se može pronaći na zapaljenim odlagalištima uglja, gdje se kondenzira iz plinova nastalih sagorijevanjem uglja. Također se može naći u nekim tipovima vulkanskih otvora. Najčešće se koristi kao gnjojivo te kao sredstvo za poboljšavanje okusa u nekim vrstama slatkiša (poput lakrica). Hemijski se dobija reakcijom hlorovodične kiseline i amonijaka.
Remove ads
Historija
Najraniji spomen amonij-hlorida zabilježen je u Kini oko 554. nove ere.[2] U to vrijeme, on se dobijao iz dva izvora: rupa i okna iz kojih je izbijao dim od zapaljenih naslaga uglja ispod površine širom Centralne Azije, a naročito ih je mnogo bilo u planinama Tian Shana kao i u Alajskim planinama u jugozapadnom Kirgistanu, dok su drugi izvor bile fumarole na vulkanu Taftan na jugoistoku današnjeg Irana.[3]
Remove ads
Dobijanje
Ovaj spoj je proizvod Solvayevog procesa, koji se koristi za dobijanje natrij-karbonata:[4]
- CO2 + 2 NH3 + 2 NaCl + H2O → 2 NH4Cl + Na2CO3
Osim što je to osnovna metoda dobijanja amonij-hlorida, ona se također koristi da bi se smanjilo ispuštanje amonijaka u okolinu tokom nekih industrijskih procesa.

U industrijskom obimu, amonij-hlorid proizvodi se miješanjem amonijaka (NH3) bilo sa plinovitim hlorovodikom ili vodenim rastvorom hlorovodične kiseline:[4]
- NH3 + HCl → NH4Cl
U prirodi se amonij-hlorid javlja u vulkanskim područjima, gdje se nakuplja na vulkanskim stijenama u blizini otvora odakle izbijaju pare (fumarole). Kristali amonij-hlorida talože se direktno iz gasovitog stanja ali nemaju duži vijek trajanja jer se lahko rastvaraju u vodi.[5]
Remove ads
Reakcije
Amonij-hlorid izgleda kao da sublimira pri zagrijavanju, međutim zapravo se raspada na amonijak i plinoviti hlorovodik.[4]
- NH4Cl → NH3 + HCl
Reagira sa jakim bazama, kao što je natrij-hidroksid, pri čemu otpušta amonijak:
- NH4Cl + NaOH → NH3 + NaCl + H2O
Na sličan način, amonij-hlorid također reagira sa karbonatima alkalnih metala pri povišenim temperaturama, dajući amonijak i hloride alkalnih metala:
- 2 NH4Cl + Na2CO3 → 2 NaCl + CO2 + H2O + 2 NH3
Rastvor od 5% amonij-hlorida u vodi (po masenom udjelu) ima pH vrijednost u rasponu od 4,6 do 6.[6] Neke reakcije amonij-hlorida sa drugim hemikalijama su endotermične, poput njegove reakcije sa barij-hidroksidom i njegovo rastvaranje u vodi.
Upotreba
Osnovna upotreba amonij-hlorida je kao izvor dušika u vidu nekog od sastojaka gnjojiva poput hloroamonij-fosfata (na šta se troši oko 90% svjetske proizvodnje amonij-hlorida). Na ovaj način uglavnom se prihranjuju žitarice poput riže i pšenice u Aziji.[7] U 18. vijeku amonij-hlorid se često koristio u pirotehničke svrhe, ali je kasnije zamijenjen mnogo sigurnijim i manje higroskopnim hemikalijama. Njegova svrha u pirotehnici bila je da otpusti hlor kako bi se poboljšale zelene i plave nijanse iona bakra u plamenu.
Osim toga, koristi se i za dobijanje bijelog dima, iako se zbog njegove reakcije dvostrukog raspadanja sa kalij-hloratom, čime se dobija veoma nestabilan amonij-hlorat, njegova upotreba smatra vrlo sumnjivom.[8][9][10]
Remove ads
Reference
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads