Sulfid fosforečný
chemická sloučenina From Wikipedia, the free encyclopedia
Remove ads
Sulfid fosforečný (P2S5) je anorganická sloučenina. Je sirným analogem oxidu fosforečného.
Stejně jako P2O5 vytváří dimerní molekuly (P4S10). Jedná se o žlutou pevnou látku, často ovšem bývá znečištěn různými příměsemi, které jej zbarvují do nazelenavě žluté barvy.
Remove ads
Struktura a příprava
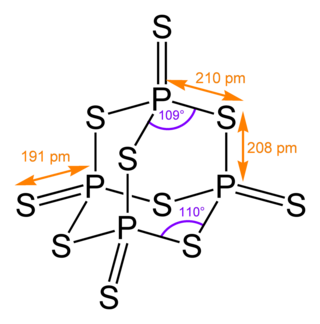
Struktura
Tato sloučenina má tetraedrickou strukturu podobnou adamantanu, která je téměř totožná se strukturou oxidu fosforečného.[2]
Příprava
Sulfid fosforečný je připravován reakcí kapalného bílého fosforu se sírou při teplotách nad 300 °C:
P4 + 10 S → P4S10.
Poprvé jej takto připravil Berzelius v roce 1843.[3]
Alternativně může být připraven reakcí elementární síry nebo pyritu (FeS2) s fosfidem železa (Fe2P):
4 Fe2P + 18 S → P4S10 + 8 FeS
4 Fe2P + 18 FeS2 + teplo → P4S10 + 26 FeS.
Remove ads
Použití
Ročně je vyrobeno přibližně 150 000 tun sulfidu fosforečného.
Ten se nejčastěji převádí na ostatní deriváty, například dithiofosforečnany zinku, které se používají jako mazací aditiva.
Rovněž se používá na výrobu pesticidů, jako jsou například parathion a malathion.[4] Je také složkou některých amorfních pevných elektrolytů pro některé typy lithiové články.
Také může být použit pro výrobu VX.
Remove ads
Reaktivita
Z důvodu hydrolýzy vzdušnou vlhkostí sulfid fosforečný vyvíjí H2S, kromě toho také vzniká kyselina fosforečná:
P4S10 + 16 H2O → 4 H3PO4 + 10 H2S.
V organické chemii se používá jako thionační činidlo.
Odkazy
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads