TEMPO
chemická sloučenina From Wikipedia, the free encyclopedia
Remove ads
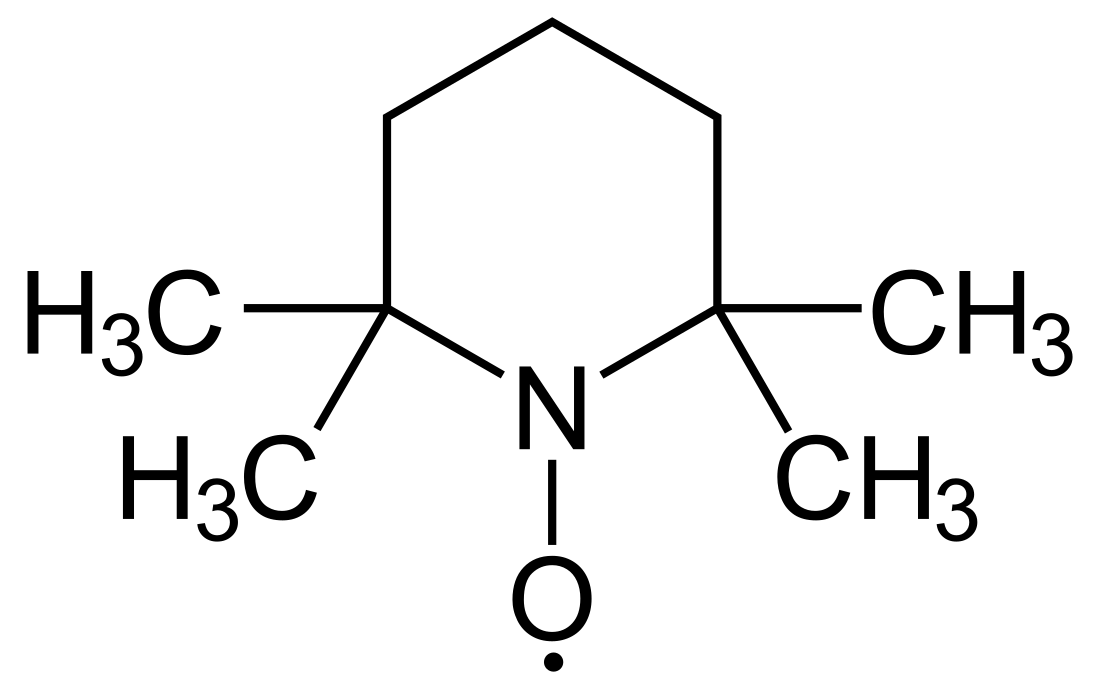
(2,2,6,6-tetramethylpiperidin-1-yl)oxyl neboli (2,2,6,6-tetramethylpiperidin-1-yl)oxidanyl, zkráceně TEMPO, je organická sloučenina se vzorcem (CH2)3(CMe2)2NO. Jedná se o červenooranžovou pevnou látku, která může sublimovat. Jde o stabilní aminoxylový radikál, s využitím v chemii a biochemii.[2]
TEMPO se používá při zkoumání biologických systémů. kde se spojuje s elektronovou paramagnetickou rezonancí, jako činidlo v organické syntéze a v radikálových polymerizacích.[3]
Remove ads
Příprava
TEMPO se připravuje oxidací 2,2,6,6-tetramethylpiperidinu.
Struktura

Struktura TEMPO byla určena rentgenovou krystalografií. Čtveřice methylových skupin radikál chrání.
Stabilitu radikálu způsobuje delokalizace radikálu, která vytváří mezi atomy N a O tříelektronovou vazbu. Stabilizace je podobná jako u oxidu dusnatého a dusného. Další stabilitu vytváří sterické efekty čtveřice methylových skupin navázaných na aminoxyl. Tyto methyly jsou inertními substituenty, zatímco každé methinové (CH) centrum vedle aminoxylu by jím bylo odštěpováno.[5]
Bez ohledu na příčiny stability radikálu jsou vazby O–H u hydrogenovaného derivátu (hydroxylaminové sloučeniny, 1-hydroxy-2,2,6,6-tetramethylpiperidinu) TEMPO–H slabé; s disociačními energiemi kolem 290 kJ/mol} asi o 30 % slabší než obvyklá vazba O–H.[6]
Remove ads
Použití v organické syntéze
Podrobnější informace naleznete v článku Oxoamoniové oxidace.
TEMPO se používá v organické syntéze jako katalyzátor oxidací primárních alkoholů na aldehydy; aktivním oxidantem je zde N-oxoamonná sůl; vzniklá při použití chlornanu sodného jako stechiometrického oxidačního činidla reakcí kyseliny chlorné s TEMPO.

Jako příklad může sloužit oxidace (S)-(−)-2-methyl-butan-1-olu na (S)-(+)-2-methylbutanal:[7] 4-methoxyfenethylalkohol se může oxidovat na příslušnou karboxylovou kyselinu systémem obsahujícím katalytické množství TEMPO a chlornanu sodného a stechiometrický chloritan sodný.[8] Oxidace pomocí TEMPO jsou chemoselektivní, protože nepůsobí na sekundární alkoholy, ale mohou převádět aldehydy na karboxylové kyseliny.
Sekundární alkoholy se pomocí TEMPO lépe oxidují v kyselém prostředí, protože pak snadněji poskytují vodíkové ionty.[9]
Když sekundární oxidační činidla vyvolávají vedlejší reakce, tak lze TEMPO stechiometricky přeměnit na oxoamonnou sůl, například při oxidaci geraniolu na geranial se nejprve oxiduje 4-acetamido-TEMPO na tetrafluorboritan oxoamonia.[10]
TEMPO je možné zapojit i do nitroxidových radikálových polymerizací (NMP), což jsou řízené radikálové polymerizace umožňující ovládat rozdělení molekulových hmotností produktů. TEMPO se může navázat na konec rostoucího řetězce polymeru, čímž vytvoří „spící“ řetězec a zastaví polymerizaci. Vazba mezi TEMPO a polymerním řetězcem je ovšem slabá a může být narušena, například zahřátím, čímž lze polymerizaci znovu spustit. Je tak možné řídit míru polymerizace a získat řetězce s úzkým rozdělením.
Použití v průmyslu a analogy
TEMPO je dostatečně levné, aby se dalo používat v laboratořích.[11] Existují i průmyslové procesy, do kterých se TEMPO zapojuje.[12]
Jsou známy i další sloučeniny s podobnou strukturou, převážně založené na 4-hydroxy-TEMPO (TEMPOL). Tato sloučenina se získává z acetonu a amoniaku přes triacetonamin, čímž se snižuje nákladnost. K dalším alternativám patří komplexy TEMPO s polymery, ty jsou recyklovatelné.[13]
K příkladům využití TEMPO a podobných sloučenin v průmyslu patří mimo jiné stabilizátory aminů a inhibitory polymerizace.
Remove ads
Odkazy
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads