Top-Fragen
Zeitleiste
Chat
Kontext
Ammoniumchromat
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Remove ads
Ammoniumchromat ist das Ammoniumsalz der Chromsäure mit der Summenformel (NH4)2CrO4.
Remove ads
Eigenschaften
Ammoniumchromat liegt in Form gelber, gut wasserlöslicher Kristalle vor, welche sich bei 185 °C explosionsartig zu Ammoniak, Stickstoff, Chrom(III)-oxid und Wasser zersetzen.[1] Des Weiteren kann Ammoniumchromat, aufgrund seiner oxidierenden Eigenschaften, auf gefährliche Weise mit Reduktionsmitteln oder brennbaren Stoffen reagieren. Wässrige Lösungen reagieren neutral.
Herstellung
Auflösung von Chrom(VI)-oxid in einer Ammoniaklösung:
Remove ads
Verwendung
Ammoniumchromat findet Verwendung bei der Herstellung von Eisen-Chromoxid-Katalysatoren.[4] Außerdem kann Ammoniumchromat zur Darstellung von Bleichromat dienen.
Sicherheitshinweise
Ammoniumchromat ist als krebserzeugend insbesondere bei Aufnahme über die Atemwege eingestuft.[1] Hautkontakt kann zu Sensibilisierung führen. Bei der Handhabung ist daher entsprechende Schutzkleidung zu tragen.
Gesetzliche Hinweise
Ammoniumchromat unterliegt der Chemikalienverbotsverordnung und dem Wasserhaushaltsgesetz. In industriellen Mengen unterliegt es außerdem der Störfallverordnung.
Ökotoxikologisch ist Ammoniumchromat als WGK 3 (stark wassergefährdend) eingestuft.[1]
Einzelnachweise
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads

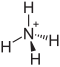
![{\displaystyle \mathrm {\ \!\ {\Biggr ]}_{2}} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/574adab1409cb81da6c38bb738ad111e61bbb2d9)

![{\displaystyle \mathrm {\ \!\ {\Biggr ]}} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/c9fd9553a0b623f5f669641be907d9186e35b739)




