
Αιθένιο
χημική ένωση / From Wikipedia, the free encyclopedia
Το αιθένιο (αγγλικά ethene) ή αιθυλένιο (αγγλικά ethylene) είναι οργανική ένωση, που περιέχει άνθρακα και υδρογόνο, με συντακτικό τύπο C2H4, αν και παριστάνεται συχνά πιο αναλυτικά με τον ημισυντακτικό τύπο του, CH2=CH2, ή και συντομογραφικά ως ViH. Πιο συγκεκριμένα, το αιθένιο είναι το απλούστερο αλκένιο, δηλαδή αλειφατικός ακόρεστος υδρογονάνθρακας με έναν διπλό δεσμό. Το χημικά καθαρό αιθένιο, στις «κανονικές συνθήκες περιβάλλοντος», δηλαδή σε θερμοκρασία 25 °C και υπό πίεση 1 atm, είναι άχρωμο εύφλεκτο αέριο με μια απαλή «γλυκιά και μοσχοβολιστή» οσμή[2].
| Αιθένιο | |||
|---|---|---|---|
 | |||
 | |||
 | |||
| Γενικά | |||
| Όνομα IUPAC | Αιθένιο Δικαρβένιο | ||
| Άλλες ονομασίες | Αιθυλένιο Διμεθυλένιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C2H4 | ||
| Μοριακή μάζα | 28,05 amu | ||
| Σύντομος συντακτικός τύπος | CH2=CH2 | ||
| Συντομογραφίες | ViH | ||
| Αριθμός CAS | 74-85-1 | ||
| SMILES | C=C | ||
| InChI | 1/C2H4/c1-2/h1-2H2 | ||
| Αριθμός EINECS | 200-815-3 | ||
| Αριθμός RTECS | KH3800000 | ||
| ChemSpider ID | 6085 | ||
| Δομή | |||
| Διπολική ροπή | 0 D | ||
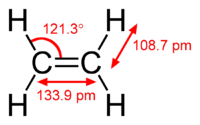
| Μήκος δεσμού | C-H: 108,7 pm C-C: 133,9 pm | ||
| Είδος δεσμού | C-H: ελαφρά πολωμένος ομοιοπολικός δεσμός σ (1s-2sp2) C-C: ομοιοπολικός δεσμός σ (2sp2-2sp2) π (2p-2p) | ||
| Πόλωση δεσμού | C-H: 3% | ||
| Γωνία δεσμού | HCC: 121,3° | ||
| Μοριακή γεωμετρία | επίπεδη (D2h) | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | -169,2 °C | ||
| Σημείο βρασμού | -88,6 °C | ||
| Κρίσιμη θερμοκρασία | 9,4 °C | ||
| Κρίσιμη πίεση | 49,9383173 atm | ||
| Πυκνότητα | 1,178 kg/m3 (15 °C) | ||
| Διαλυτότητα στο νερό | 2,9 g/m3 | ||
| Τάση ατμών | 40 atm (-1,5 °C) | ||
| Εμφάνιση | Άχρωμο αέριο | ||
| Χημικές ιδιότητες | |||
| pKa | 44 | ||
| Θερμότητα πλήρους καύσης | 1314 kJ/mole | ||
| Βαθμός οκτανίου | 97,3[1] | ||
| Ελάχιστη θερμοκρασία ανάφλεξης | -136 °C | ||
| Σημείο αυτανάφλεξης | 542,8 °C | ||
| Επικινδυνότητα | |||
 | |||
| Εξαιρετικά εύφλεκτο (F+) | |||
| Κίνδυνοι κατά NFPA 704 | |||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Από τότε που το πετρέλαιο έγινε η πλέον «στρατηγική» πρώτη ύλη του πλανήτη μας, το αιθένιο έγινε επίσης η «κεντρική» οργανική πρόδρομη ένωση, αφού χρησιμοποιείται ευρύτατα από τη χημική βιομηχανία, αποτελώντας την κυριότερη βάση από την οποία παράγονται πλήθος πρωτογενών ή και δευτερογενών προϊόντων, όπως το πολυαιθυλένιο, το οξιράνιο, το στυρόλιο ή και άλλες α-ολεφίνες. Η ετήσια παγκόσμια παραγωγή του, που ήταν πάνω από 109 εκατομμύρια τόννοι το 2006, ξεπέρασε τελικά κάθε άλλη βιομηχανικά παραγώμενη οργανική ένωση[3][4].
Το 2016, παρά την οικονομική κρίση που προηγήθηκε, η παγκόσμια παραγωγή του ξεπέρασε τους 150 εκατομμύρια τόννους. Μεγάλο μέρος της παραγωγής του κατευθύνεται προς την παραγωγή πολυαιθυλενίου, που με τη σειρά του αποτελεί ένα ευρύτατα χρησιμοποιοποιούμενο είδος πλαστικού, που περιέχει αλυσίδες αιθενίου διαφόρων μηκών. Η παραγωγή αυτή εκλύεει αέρια του θερμοκηπίου, που συμπεριλαμβάνουν μεθάνιο ως παραπροϊόν της παραγωγής αιθενίου και διοξείδιο του άνθρακα, από την παραγωγή ενέργειας που απαιτείται για την παραγωγή κάθε επιμέρους συστατικό που χρησιμοποιείται για τη διεργασία παραγωγής.
Στην Ευρώπη και στην Ασία το αιθένιο παράγεται βιομηχανικά με ατμοπυρόλυση αργού πετρελαίου ή και βενζίνης, αλλά στις ΗΠΑ και στον Καναδά προτιμάται η ατμοπυρόλυση αιθανίου, προπανίου ή και υγραερίου, γενικότερα.
Το αιθένιο είναι, επίσης, μια σημαντική φυσική φυτική ορμόνη, που χρησιμοποιείται με φυσικό τρόπο από τα φυτά και με τεχνητό τρόπο στην αγροτική παραγωγή για να δώσει την εντολή για την ωρίμανση των φρούτων[5].
